
| A. | 0.30g | B. | 0.20g | C. | 0.15g | D. | 0.45g |
分析 锌粉、铝粉、镁粉的混合物3.8g与一定质量的稀硫酸恰好完全反应,生成硫酸锌、硫酸铝、硫酸镁混合物11g,根据反应前后元素质量不变,则硫酸锌、硫酸铝、硫酸镁三种物质的混合物中含硫酸根的质量为11g-3.8g=7.2g;根据硫酸中氢与硫酸根的比,计算出氢元素的质量,即产生氢气的质量.
解答 解:根据反应前后元素质量不变,反应生成的11g硫酸锌、硫酸铝、硫酸镁混合物中含有硫酸根的质量=11g-3.8g=7.2g;根据硫酸的化学式H2SO4,其中氢元素与硫酸根的质量比=2:96=1:48,当硫酸中所含硫酸根的质量为7.2g时,硫酸中H元素的质量=7.2g×$\frac{1}{48}$=0.15g,即反应中产生的氢气质量为0.15g;
故选C.
点评 本题的解决技巧在于:由金属和硫酸根所组成的硫酸盐中,除去金属余下的就是硫酸根.


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:初中化学 来源: 题型:实验探究题
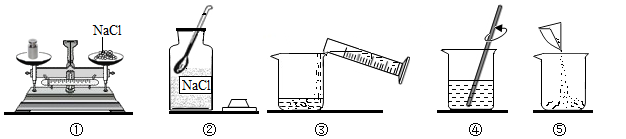
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
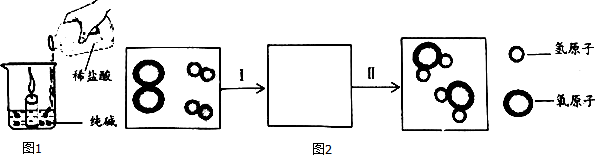
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
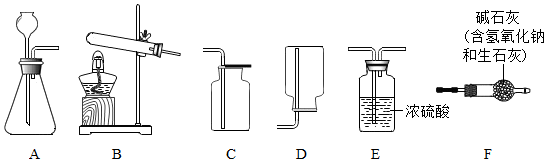
| 物质 | NaHCO3 | NH4Cl |
| 溶解度/g(20℃) | 9.6 | 37.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
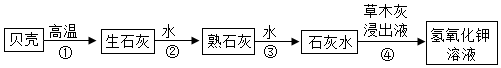
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
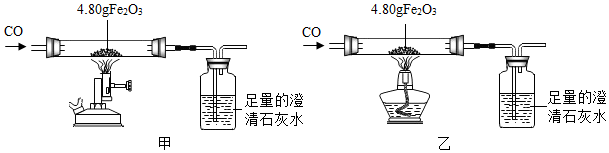
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 称量黑色粉末质量/g | m1 | m2 |
| 2 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
| 3 | 取黑色粉未,加入稀盐酸 | 全部溶解,有大量气泡 | 无明显现象 |
| 4 | 取黑色粉末,加入足量CuSO4溶液 | 有红色物质生成 | 无明显现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com