
【题目】根据如图所示的实验操作回答问题。

(1)甲图装置中的一处错误是______;
(2)某同学用乙图装置探究燃烧的条件,水的作用是提供热量和______;
(3)丙实验燃烧匙中所盛药品红磷要过量,其原因是______;
(4)丁图中硬质玻璃管内发生反应的化学方程式为______;丁图中有一处明显的缺陷,请指出______。
【答案】大拇指按在试管夹的短柄上 隔绝氧气 为了将装置内的氧气完全耗尽 3CO+Fe2O3![]() 2Fe+3CO2 没有对尾气进行处理
2Fe+3CO2 没有对尾气进行处理
【解析】
(1)给试管中的液体加热时,大拇指不能按在短柄上,以防试管脱落造成试管破裂。甲图装置中的一处错误是大拇指按在试管夹的短柄上;
(2)乙图装置中水的作用是提供热量和隔绝氧气;
(3)测定空气中氧气的含量时,为了将装置内的氧气完全耗尽,燃烧匙中所盛药品红磷要过量;
(4)一氧化碳具有还原性,在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;一氧化碳有毒,该装置没有对尾气中的一氧化碳进行处理,会造成空气污染。丁图中有一处明显的缺陷是没有对尾气进行处理。
2Fe+3CO2;一氧化碳有毒,该装置没有对尾气中的一氧化碳进行处理,会造成空气污染。丁图中有一处明显的缺陷是没有对尾气进行处理。


科目:初中化学 来源: 题型:
【题目】科学家发现用氨气(NH3)可以将NO转化成无毒物质直接排放,反应的微观示意图如下。
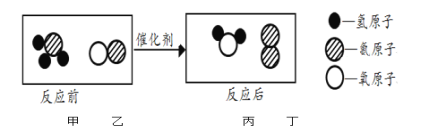
从图中获得的有关信息不正确的是
A. 甲中氮、氢原子个数比为1:3
B. 乙的相对分子质量为30
C. 反应前后分子种类不变
D. 生成物水和氮气的分子个数比为6:5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图(省略夹持装置),回答下列问题、

(1)仪器⑤的名称是___________。
(2)实验室用氯酸钾制备氧气的化学方程为_______,发生装置应选择仪器________,(填序号,下同),收集一瓶氧气来进行硫燃烧的实验,则应选择的仪器为____________。
(3)用大理石和稀盐酸制取二氧化碳,组装一套能控制反应发生和停止的发生装置,应选择仪器_____,若要控制反应的速度,则应用_____代替⑤。
(4)氮化铝(AlN)是新型的电子绝缘基片材料,用于大型和超大型集成电路中,下图为在高温下氮气、碳氧化铝反应生成氮化铝和一氧化碳的装置。(氮化铝与水会发生反应)
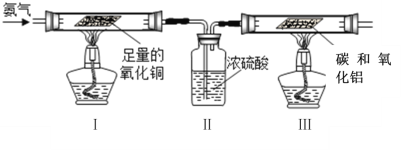
装置Ⅰ用于制取N2,同时氧化铜被还原,该反应的化学方程式为__________
装置Ⅱ的作用是___________________。
实验结束后先熄灭__________(填“Ⅰ”或“Ⅲ”)处的酒精灯。该装置有缺陷,改进的方法是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是四种物质的溶解度曲线图,请回答下列问题。

(1)在60℃时,四种物质中溶解度最大的是 。
(2)将40℃时氯化钾的不饱和溶液,保持溶液温度不变,制成饱和溶液,可行的方法有 (举1例)。
(3)在t℃时,将30g氯化铵加入50g水中,充分溶解,所得溶液质量分数为 (精确到0.1%)。
(4)向饱和食盐水中加入足量的碳酸氢铵固体,会有溶解度较小的碳酸氢钠晶体析出,该反应的化学方程式是NaCl+NH4HCO3 =NaHCO3↓+NH4Cl,请根据以上信息和题13图中物质的溶解度曲线,简述以硫酸铵固体为原料制取较纯硫酸钾晶体的方法: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图A是某粒子的结构示意图,B是铝元素周期表中的信息。请回答下列问题:
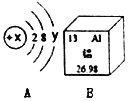
(1)若A粒子带有两个单位的负电荷,且y等于8,则该粒子的符号为______;
(2)当x=17时,A元素和B元素形成的化合物化学式______;
(3)B元素的单质在空气中能生成致密的______(化学式)薄膜;
(4)从B中可知,铝的相对原子质量为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a,b两种物质的溶解度曲线如图所示,下列说法正确的是 ( )

A. a物质的溶解度大于b物质的溶解度
B. t1℃时,a,b两溶液的溶质质量分数相等
C. 将t2℃时a的饱和溶液降温至t1℃,溶液质量不变
D. 将t1℃时,a、b物质的饱和溶液升温至t2℃时,两溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国是把香椿当做蔬菜的唯一国家,它不仅营养丰富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙属于_______________(填“有机物”或“无机物”);
(2)皂甙中各元素的质量之比是____________________(最简整数比);
(3)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:请你仔细分析此关系图,并进行计算。
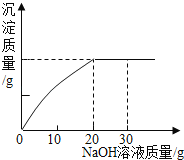
(1)当滴入氢氧化钠溶液_____g时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液的溶质的质量分数(写出计算过程)。__________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com