
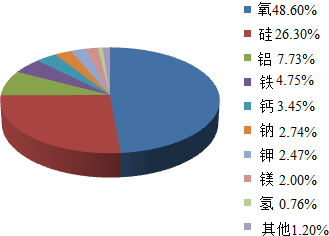
 如图表示的是地壳里所含各种元素的质量分数.请据图回答下列问题;
如图表示的是地壳里所含各种元素的质量分数.请据图回答下列问题;科目:初中化学 来源: 题型:选择题
| A. | 空气中的氧气可以供给呼吸、燃烧、炼钢、化工生产等 | |
| B. | 雨润香肠采用真空包装的主要目的是为了隔绝氧气 | |
| C. | 在测定空气中氧气含量的实验中,选用的红磷要足量 | |
| D. | PM2.5是造成空气污染的主要污染物之一 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源:南京市高淳县2017届九年级中考二模化学试卷 题型:选择填充题
除去下列各物质中混有的少量杂质,所用的试剂或操作不合理的是
选项 | 物质 | 杂质 | 试剂、方法 |
A | 二氧化碳 | 一氧化碳 | 通过灼热的氧化铜 |
B | 木炭粉 | 铁粉 | 用磁铁吸引 |
C | NaOH溶液 | Na2CO3 | 加入过量Ba(OH)2溶液,过滤 |
D | 氧化铜 | 铜粉 | 在空气中灼烧 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源:【全国市级联考】安徽省合肥市2017届九年级中考第一次模拟考试化学试卷 题型:探究题
实验小组的同学欲对碳还朱氧化铜生成的气体成分进行探究。
[提出猜想]气体成分为①只有CO,②只有CO2,③CO和CO2的混合气体。得出以上猜想的依据是___________。
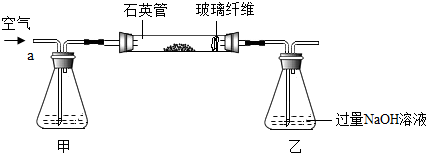
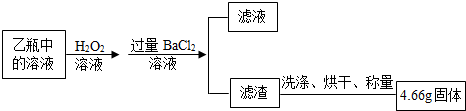
[实验设计](1)将生成的气体通入如图装置一段时间,发现C中液体变浑浊,由此排除了猜想____(填序号)。

(2)先通气体一会后,点燃酒精灯,先预热,后对准玻璃管中的氧化铜加热,出现______现象,说明猜想③成立。
[交流与讨论](1)将生成气体通入装置一段时间再加热,除探究CO2存在外,还能达到的目的是_________________________。
(2)请写出一个该实验产生CO可能发生的化学反应的化学方程式______________。
装置B可以防止液体回流使玻璃管炸裂,装置C的作用是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com