
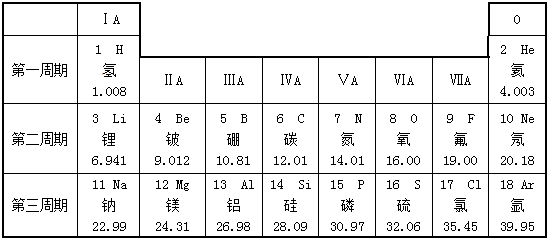
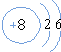 ,该微粒是元素周期表中的氧元素,核电荷数是8,碳元素的核电荷数是6,因此不同元素的本质区别是核电荷数不同.
,该微粒是元素周期表中的氧元素,核电荷数是8,碳元素的核电荷数是6,因此不同元素的本质区别是核电荷数不同.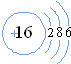 ,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.
,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.分析 (1)根据原子序数等于核电荷数以及元素的概念进行分析;
(2)根据硫元素的原子结构示意图进行分析;
(3)根据核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子,阴离子可能是氧离子、氟离子等进行解答.
(4)根据元素周期数与电子层数的关系、同一周期原子核外电子排布的变化进行分析解答;
(5)根据在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束进行解答.
解答 解:(1)通过分析微粒的结构示意图可知,原子核内有8个质子,所以微粒是元素周期表中的氧元素,核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是:核电荷数不同;故填:氧,8,6,核电荷数不同;
(2)从硫原子的核外电子排布可以看出,硫原子在化学反应中易得电子,是非金属元素.故填:得,非金属;
(3)核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子,阴离子可能是氧离子、氟离子;故填:Na+;O2-.
(4)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加;故填:原子核外电子层数相同;最外层电子数依次增加;
(5)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束;故填:金属;非金属.
点评 本题考查元素周期律的实质和元素周期表的用途,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键.


 全能练考卷系列答案
全能练考卷系列答案科目:初中化学 来源: 题型:解答题
 水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:如图所示,实验Ⅰ是制备蒸馏水的装置,实验Ⅱ是电解水的装置.
水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:如图所示,实验Ⅰ是制备蒸馏水的装置,实验Ⅱ是电解水的装置.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中正确的是A
现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中正确的是A查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 利用水、天平和量筒测密度 | B. | 浸入稀盐酸中观察有无气泡产生 | ||
| C. | 浸入CaCl2溶液中观察 | D. | 浸入CuSO4溶液中观察是否变色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com