
【题目】为除去氯化钠中的泥沙和CaC12、MgCl2、Na2SO4杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。

(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是_____。
(2)写出一个加入Na2CO3溶液时所发生反应的化学方程式_____。
(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含哪些杂质?_____(BaSO4不溶于水,也不溶于酸)
【答案】玻璃棒 Na2CO3+CaCl2═CaCO3↓+2NaCl或BaCl2+Na2CO3═BaCO3↓+2NaCl 氯化钙、氯化镁、氯化钡
【解析】
氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,和氯化钡反应生成白色沉淀碳酸钡和氯化钠;盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,和氢氧化镁反应生成氯化镁和水,和碳酸钡反应生成氯化钡、水和二氧化碳。
(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是玻璃棒。
(2)加入Na2CO3溶液时,碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,和氯化钡反应生成白色沉淀碳酸钡和氯化钠,发生反应的化学方程式![]() ,
,![]() 。
。
(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,和氢氧化镁反应生成氯化镁和水,和碳酸钡反应生成氯化钡、水和二氧化碳,所得精盐产品中杂质有氯化钙、氯化镁、氯化钡。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】自然界并不缺少镁,缺少的是发现镁的眼睛。某化学兴趣小组开启寻镁之旅,现邀请你参与并完成相关内容。
(1)第一站:初识金属镁。(①金属镁的物理性质:____(写一条);②金属镁的化学性质:镁能与氧气反应,反应的化学方程式为___.
(2)第二站:再遇金属镁。将打磨过的镁条放入稀盐酸中,反应现象是______。化学方程式为______。
(3)第三站:制备金属镁。小组同学模拟工业上从海水晒盐剩下的苦卤中提取镁,流程如下:
![]()
流程中X为________________.
(4)第四站:再探金属镁。
(提出问题)镁能否与热水反应?如果反应,产物是什么?
(相关信息)①Mg+2H2O=Mg(OH)2+H2↑②氢氧化镁在热水中能部分溶解。
实验操作 | 实验现象 | 实验结论 |
______ | _____ | 镁能与热水反应,生成氢氧化镁和氢气 |
(5)上述寻镁之旅中你收获到镁的化学性质有_______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,是国际通用语言,请用适当的化学用语填空。
(1)氦气:_____
(2)两个镁离子:_____
(3)4个硫原子:_____
(4)五氧化二磷中磷元素化合价为+5价_____:
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向10g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。
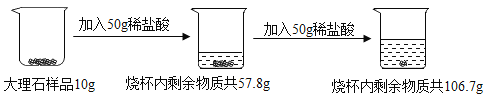
请计算:
(1)该大理石样品中碳酸钙的质量分数是_____;
(2)计算所用稀盐酸的溶质质量分数;_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】质量相等的四种物质①H2O2②KMnO4③KClO3④H2O,完全分解后所制得氧气的质量由大到小的顺序为_____(填序号,下同);四种金属①Zn②Mg③Al④Fe分别投入质量相等且足量的稀硫酸中,充分反应后所得四种溶液的质量相等,则投入金属的质量由小到大的顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现欲探究一固体混合物A的成分,已知其中可能含有Na2SO4、Na2CO3、CuO、NH4Cl四种物质中的两种或多种。按图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行)。
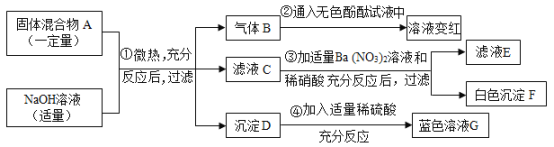
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体B的水溶液显________。(选填“酸性”、“碱性”、“中性”之一)
(2)写出步骤③中生成白色沉淀F的化学方程式为________________。
(3)滤液E中一定存在酸根离子符号为________________。
(4)混合物A中,一定不存在的物质是________________,理由是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小红家从农贸市场买回一包化肥,化肥包装上的标签如图所示,请回答下列问题。

(1)该化肥是由_____种元素组成的。
(2)该化肥中C、N两种元素的质量比是_____。
(3)试通过计算说明此种尿素的纯度____(是、否)为一级品?(国际一级品标准为尿素的质量分数98.5%),
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:Al(OH)3沉淀可溶于NaOH溶液,其反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
现向100g HCl和AlCl3的混合溶液中逐滴加入质量分数为20﹪的NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示。回答下列问题:

(1)原混合溶液中HCl的质量分数是______。
(2)当沉淀达到最大值时生成NaCl的质量是_____?
(3)m2=____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com