解:(1)①举一个分子运动的事例,能体现分子在不断的运动着;如:墙内开花墙外香;
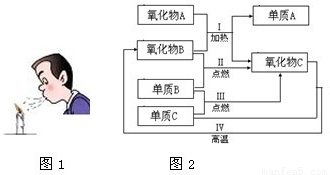
②根据如图1实验,分析蜡烛熄灭的原因使温度降到着火点以下;
③金刚石和石墨都是由碳元素组成,金刚石硬度大且不能导电,而石墨却很软且导电性好,它们物理性质差异大的原因是碳原子的排列方式不同;
④电解水时正极产生了10mL气体,根据氧气和氢气体积为1:2,则负极产生的气体体积是20mL,该实验能够说明水是由氢元素与氧元素组成的理论依据是化学反应前后元素的种类不变;
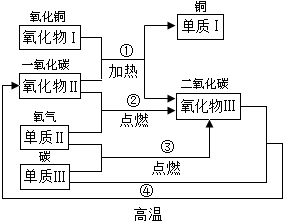
(2)由于氧化物III能够使澄清石灰水变浑浊,所以氧化物III为二氧化碳.而氧化物II和单质II点燃能够生成二氧化碳,所以单质II一定是氧气,而氧化物II一定为一氧化碳.同时单质II(已经确定为氧气)和单质III反应能够生成二氧化碳(氧化物III),所以单质III为碳.氧化物III(二氧化碳)和单质III(碳)也能在高温的情况下生成氧化物II(一氧化碳).氧化物I和氧化物II(一氧化碳)反应生成单质I(红色固体)和氧化物III(二氧化碳),所以单质I为铜,而氧化物I为氧化铜,黑色固体.这样就符合所有的限制条件.结论为:
①在反应①中CuO+CO

Cu+CO
2.在反应中CuO失去氧,做氧化剂,发生的是还原反应.
②氧化物II为一氧化碳,在给定的转化中,在反应①体现的是还原性(反应为CuO+CO

Cu+CO
2),在②中体现的可燃性(反应为2CO+O
2
2CO
2).所以没有涉及到的为毒性,危害人类健康.
③反应④是二氧化碳字高温下和碳反应生成一氧化碳.其反应方程式为:CO
2+C

2CO.该反应过程中吸收热量.
故答案为:(1)①墙内开花墙外香;②使温度降到着火点以下;③碳原子的排列方式不同;④20mL;化学反应前后元素的种类不变;
(2)①CuO;
②毒;
③CO
2+C

2CO.吸收.
分析:(1)根据分子运动的事例、灭火的原理气体发生装置的确定、物质的性质一一分析.
(2)本题给的图好像很复杂的样子,其实就是涉及6种物质,所以不要被先入为主吓倒.单质I为红色固体,在红色物质中只有铜是单质固体.而氧化物I和单质III均为黑色固体,黑色单质应该是碳,而黑色氧化物且能对应金属铜的只能为氧化铜.而氧化物III能够使澄清石灰水变浑浊,则氧化物III为二氧化碳.
点评:考查知识面较多,要明确每一题的信息,逐一解答.



 Cu+CO2.在反应中CuO失去氧,做氧化剂,发生的是还原反应.
Cu+CO2.在反应中CuO失去氧,做氧化剂,发生的是还原反应. Cu+CO2),在②中体现的可燃性(反应为2CO+O2
Cu+CO2),在②中体现的可燃性(反应为2CO+O2 2CO2).所以没有涉及到的为毒性,危害人类健康.
2CO2).所以没有涉及到的为毒性,危害人类健康. 2CO.该反应过程中吸收热量.
2CO.该反应过程中吸收热量. 2CO.吸收.
2CO.吸收.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
 (1)在化学学习中,我们要学会“透过现象看本质”去认识物质和变化.
(1)在化学学习中,我们要学会“透过现象看本质”去认识物质和变化.