
【题目】实验室加热3.16g高锰酸钾固体制备氧气,加热一段时间后剩余固体混合物3g,继续加热至高锰酸钾完全反应,再将固体加水充分溶解、过滤、干燥得到0.87 g黑色固体。求3 g剩余固体混合物中氧元素的质量
A.0.08g
B.0.16g
C.0.32g
D.1.12g
科目:初中化学 来源: 题型:
【题目】学习了二氧化锰对过氧化氢分解有催化作用的知识后,引起了化学探究小组的兴趣。
(提出问题)氧化铜能否作过氧化氢溶液分解的催化剂?
(实验探究)
实验步骤 | 实验现象 |
I.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铜粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B中无明显现象 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃。 |
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 |
(实验结论)
(1)由实验I你可以得出的结论是_____能加快过氧化氢分解生成氧气的速率。
(2)实验Ⅱ、Ⅲ证明:氧化铜的_____和_____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)过氧化氢在氧化铜的催化下分解放出氧气反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用上题中F装置制取二氧化碳后,U型管中的残留液倒入废液缸中,某化学小组的同学想探究废液中的溶质是什么,请和他们一起来探究,并完成下列各题。
(1)(查阅资料)实验室制C的反应:![]() ,CaCl2溶液呈中性
,CaCl2溶液呈中性
(2)(提出问题)废液中的溶质是什么物质?
(3)(作出猜想)猜想一:废液中的溶质只有CaCl2,
猜想二:废液中的溶质有CaCl2和___________(填化学式)。
(4)(实验与结论)
①甲同学取少量废液加入到试管中,并向其中滴入无色酚酞溶液,观察到溶液呈无色,于是甲同学得出结论猜想一正确。你认为甲同学的实验_________(“能”或“不能”)证明猜想一正确,理由是__________。
②如果要证明猜想二正确,下列实验方案可行的是__________。
A 滴入紫色石蕊溶液
B 测溶液的pH
C 加入Na2CO3溶液
D 加入氢氧化钠溶液
(5)(拓展应用)
①实验结果证明上述猜想二正确,如果将这种废液倒入下水道,对铁管会造成腐蚀,写出废液腐蚀铁管的化学方程式__________。
②小组同学建议加入碳酸钠溶液处理废液。在往废液中加入碳酸钠溶液时,产生沉淀和气体的质量与加入碳酸钠溶液质量的关系如图所示,下列说法错误的是_____________。

A A点时对应的溶液中只有一种溶质
B O至A过程中,溶液的pH变大
C B至C的过程表示生成沉淀的过程
D OA段发生置换反应,BC段发生复分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图表示元素的化合价与物质类别的关系,“→”表示物质之间可以转化。A、B、C、D、E、F、G是初中化学所学物质,分别由H、O、S、Cl、K、Ba中的一种、两种或三种元素组成。请回答:
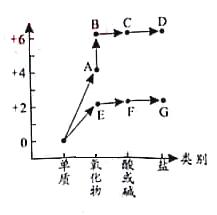
(1)A和E的化学式分别为__________和__________。
(2)D与G反应的化学方程式为__________,此反应属__________(填基本反应类型)。
(3)A—G物质间,发生中和反应的化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】18世纪末,人们就开始了对水的组成的研究。
(1)①卡文迪许把“易燃空气”(氢气)和纯氧气混合后盛在干燥、洁净的玻璃瓶中,当用电火花点火时发出震耳的爆鸣声,且玻璃瓶内壁上出现了液滴,该反应的化学方程式是_____;
②基于卡文迪许实验,可得出的关于水的组成的结论是_____;
A 水是由氢气和氧气组成的
B 水是由氢元素和氧元素组成的
C 每个水分子是由2个氢原子和1个氧原子构成的
(2)小林同学收集到一瓶浑浊的河水,他模拟自来水厂的净水过程,最终制成蒸馏水,其实验过程如图所示。请回答以下问题:
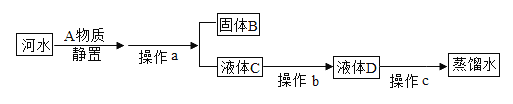
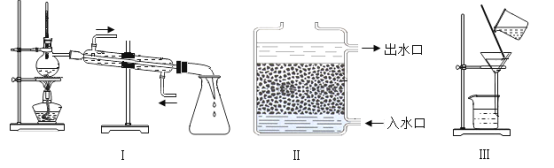
①操作a的名称是_____;进行该操作时用到铁架台、玻璃棒、烧杯、_____等仪器。
②进行操作b时,常在自制净水器中加入_____, 用于除去水中的异味和色素。
③小林取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,没有泡沫,说明液体D是_____水;操作c应选用的装置是_____(填序号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲烷(CH4) 与CO、H2的性质有诸多相似处:难溶于水、具有可燃性等。而CO、H2都能还原金属氧化物,那么甲烷(CH4)能否还原氧化铜?若能反应,产物有哪些?校兴趣小组针对于此,称取4. 0g氧化铜粉末,展开探究:

[查阅资料]①无水CuSO4为一种白色固体,其遇水变蓝;
②Cu和Cu2O均为红色固体,且![]() 。
。
[进行实验]甲同学组装装置并检查其气密性良好。通入纯净、干燥的CH4后,乙同学提醒CH4有可燃性,在点燃A处酒精喷灯前,需从C装置后尖嘴导管处收集气体并______________。D处燃着酒精灯的作用主要是处理多余的CH4,请写出发生反应的化学方程式___________。
[实验现象] A中黑色粉末逐渐变红; B中白色固体变蓝; C中澄清石灰水变浑浊。
[产物分析]结合实验现象,可以判断:甲烷能够还原氧化铜。
甲同学认为:实验后,装置A中所得红色固体全部为单质铜,并结合装置B、C实验现象,书写出甲烷与氧化铜反应完全转化为单质铜的化学方程式_______________________。
乙同学认为:实验后,装置A中所得红色固体并不一定全部为单质铜,理由是_______________________。
[定量测定]
小组同学待装置冷却后,停止通CH4,测得A中红色粉末的质量为3.4g.若CH4将4.0g,氧化铜完全还原为铜单质,则理论上所得铜单质的质量应该为_______________________;故所得红色粉末中一定含有氧化亚铜。
另一小组为进一步确定该红色粉末中氧化亚铜的质量,该小组同学将上述3.4g红色粉末置于试管中加入足量稀硫酸,加热并充分振荡,静置。观察到:红色固体逐渐减少,但未完全溶解,溶液由无色变蓝色。再将实验所得物质进行过滤、洗涤、干燥,称量,最终所得红色固体的质量为2.4g。通过计算确定原3.4g红色固体中氧化亚铜的质量(请写出计算过程)_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某石灰厂有一批石灰石原料,为了测定该石灰石的纯度,厂化验室技术员称取62.5g粉碎的石灰石粉末,进行四次高温煅烧(杂质没有变化)、冷却、称量剩余固体 质量的重复操作,记录数据如下:(提示:碳酸钙在高温下分解,生成氧化钙和二氧化碳气体)
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量 | 55.5g | 43.5g | 40.5g | 40.5g |
试计算:
(1)完全反应后生成二氧化碳_____ g;
(2)石灰石样品中碳酸钙的质量_____。有计算过程
(3)石灰石样品中碳酸钙的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙炔(C2H2)气体和氧气反应能产生高温火焰,常用于切割和焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时还生成一种白色固体。
(提出问题)白色固体是什么物质?
(做出猜想)小明经过思考认为有以下几种可能:
猜想一:CaO; 猜想二:CaCO3; 猜想三:_____。
他的依据是_____。
(交流反思)经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:_____。
(进行实验)
(一)取少量白色固体于试管中,滴加稀盐酸,没有观察到_____ ,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液,滴加_____ ,溶液变红色,证明猜想三成立。
结论:白色固体是_____。写出碳化钙与水反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自2018年1月1日起,合肥市区禁止燃放烟花爆竹,开启了霸都环保新时代。
(1)“禁止燃放烟花爆竹”的安全标志是____________。

(2)烟花爆竹的主要成分是黑火药,其化学组成为硝酸钾(KNO3)、硫磺和木炭等。黑火药中至少有_____种元素,燃放烟花爆竹时产生有刺激性气味的二氧化硫的化学方程式是_________。故禁止燃放烟花爆竹不仅可以减少噪声污染、火灾等,还可以减少二氧化硫和可吸入颗粒物等空气污染物的排放,提升空气质量。
(3)燃放烟花爆竹时还有可能引起火灾。“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭,“火立熄”的灭火原理是_________。
A 清除可燃物
B 使可燃物与空气隔绝
C 降低可燃物的着火点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com