
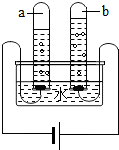
 ��2012?��ɽ��ˮ������֮Դ��Ҳ������������Դ���ش��������⣺
��2012?��ɽ��ˮ������֮Դ��Ҳ������������Դ���ش��������⣺


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ���� | ԭ�ӽṹʾ��ͼ | ���ʵ� ��ѧʽ |
���³�ѹ�� ״̬ |
������������Ӧ |
| �� | F | 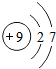 |
F2 | ��̬ | �ڰ�����ը |
| �� | Cl | 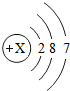 |
Cl2 | ��̬ | ���ձ�ը |
| �� | Br | 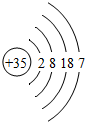 |
Br2 | Һ̬ | ���ȷ�Ӧ |
| �� | I | 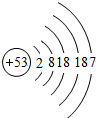 |
I2 | ��̬ | �������Ȼ�����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2012?��ɽ���ٽ��п����ҳ�Ϊ�˸�ѧ������Ӫ�����ƶ�������ʳ�ף�
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶ȡ� | 0 | 20 | 40 | 60 | 80 | 100 |
| �ܽ��/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
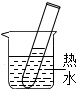 ��1��20��ʱ����װ��5g KNO3������Թ��У�����10gˮ���������ʱ������ҺΪ
��1��20��ʱ����װ��5g KNO3������Թ��У�����10gˮ���������ʱ������ҺΪ�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com