
 ij����������ԱС������Ȼ������Ȼ�����ɵIJ�Ʒ���Ȼ��Ƶ�����������ȡ16.25g������Ʒȫ������143.6gˮ�У���������Һ�еμ�������������Ϊ10.6%��̼������Һ����¼����ͼ��ʾ�����߹�ϵ��
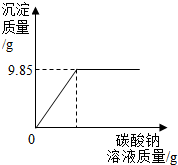
ij����������ԱС������Ȼ������Ȼ�����ɵIJ�Ʒ���Ȼ��Ƶ�����������ȡ16.25g������Ʒȫ������143.6gˮ�У���������Һ�еμ�������������Ϊ10.6%��̼������Һ����¼����ͼ��ʾ�����߹�ϵ������ ��ͼ�п�֪�����ɳ���̼�ᱵ��������9.85g�����ݳ������������Լ���̼���Ƶ����������ɵ��Ȼ��Ƶ���������һ�����Լ�������10.6%��̼������Һ����������Ʒ���Ȼ��Ƶ�������������������Һ�����ʵ�����������
��� �⣺��ǡ����ȫ��Ӧʱ̼���Ƶ�����Ϊx���Ȼ���������Ϊy����Ӧ�����Ȼ��Ƶ�����Ϊz��
Na2CO3+BaCl2�TBaCO3��+2NaCl��
106 208 197 117
x y 9.85g z
$\frac{106}{x}$=$\frac{208}{y}$=$\frac{197}{9.85g}$=$\frac{117}{z}$��
x=5.3g��y=10.4g��z=5.85g��
���Ȼ�����̼����ǡ����ȫ��Ӧʱ������10.6%��̼������Һ������Ϊ��5.3g��10.6%=50g��
�𣺵��Ȼ�����̼����ǡ����ȫ��Ӧʱ������10.6%��̼������Һ��������50g��
��2����Ʒ���Ȼ��Ƶ���������Ϊ��$\frac{16.25g-10.4g}{16.25g}$��100%=36%��
�𣺲�Ʒ���Ȼ��Ƶ���������Ϊ36%��
��3����Һ�������Ȼ��Ƶ�����Ϊ��16.25g-10.4g+5.85g=11.7g��
��Һ����Ϊ��16.25g+143.6g+50g-9.85g=200g��
����������Һ�����ʵ���������Ϊ��$\frac{11.7g}{200g}$��100%�T5.85%��
�𣺹���������Һ�����ʵ���������Ϊ5.85%��
���� �����ۺϷ�����Һ����ʱ����Ҫ©����ȥ����̼�ᱵ����������Ϊ̼�ᱵ������ˮ��������Һ��һ���֣�Ҫע�����⣮


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ��ʹ��̪��Һ���ɫ������ʹ��̪��Һ���ɫ��һ���Ǽ���Һ | |
| B�� | ������������ʱ��ֻҪij��Һ�����������壬�����Һ��������������һ����С | |
| C�� | ������Һ�м����Ȼ�����Һ������ɫ������������Ȼ���������ɫ������������Һһ���������� | |
| D�� | ԭ�ӡ����Ӳ����磬�����������һ���Ƿ��Ӻ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18�� | B�� | 24�� | C�� | 12�� | D�� | 16�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���ʣ�������Ϊ���ʣ� | �������� | |
| A | CO2��HCl�� | ��ͨ��������������Һ����ͨ��Ũ���� |
| B | NaCl��Һ��Na2CO3�� | ��ϡ����ǡ�ò��ٲ�������Ϊֹ |
| C | CuSO4��Һ��H2SO4�� | �ӹ�������ͭ��ĩ��ַ�Ӧ����� |
| D | ���ۣ�ͭ�ۣ� | �ӹ���FeSO4��Һ��ַ�Ӧ����ˡ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼ�ŵľƾ��Ʋ���������������ʪ������ | |
| B�� | ������������ʱ��û�������κ����������������Ѵ��� | |
| C�� | ����100g 10%���Ȼ�����Һ��Ҫ10g �Ȼ��ƺ�100g ˮ | |
| D�� | ��pH��ֽ�ⶨ��Һ����ʱ���Ƚ�pH��ֽ��ˮ��ʪ��Ȼ���ٲⶨ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com