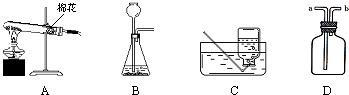
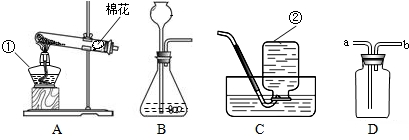
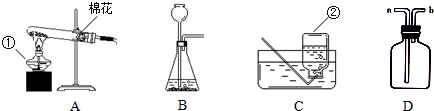
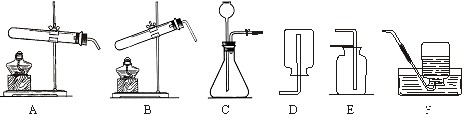
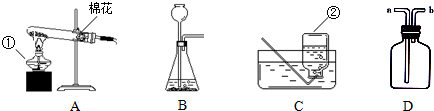
解:(1)图中标字母的仪器分别是①酒精灯;②集气瓶;
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
实验时该装置试管口应放一团棉花,其目的是:防止加热时高锰酸钾粉末随氧气流进入导管或造成堵塞;
因为氧气不易溶于水且不和水发生化学反应,所以可以采用排水法收集;
(3)用大理石和稀盐酸反应制取CO
2,产生氯化钙、水和二氧化碳,反应的方程式为:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;二氧化碳的密度比空气大,如果选用图E来收集气体,则气体应从a端进入,将空气挤压到集气瓶上部从b管排出;
故答案为:(1)①酒精灯;②集气瓶
(2)2KMnO
4
K
2MnO
4+MnO
2+O
2↑;防止高锰酸钾颗粒随气流进入导气管;氧气不易溶于水且不和水发生化学反应;
(3)CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;a.
分析:(1)熟悉常见仪器,了解名称;
(2)根据高锰酸钾加热生成锰酸钾、二氧化锰和氧气,写出反应的方程式;根据制取氧气时的注意事项分析棉花的作用;根据氧气的溶解性分析用排水法收集的原因;
(3)根据制取二氧化碳的药品及反应条件书写反应原理,并结合二氧化碳的密度及图示分析解答进气口.
点评:本考点主要考查氧气和二氧化碳的制取装置和收集装置的选择,同时也考查了化学方程式的书写和实验的注意事项,综合性比较强.关键是明确气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; K2MnO4+MnO2+O2↑;防止高锰酸钾颗粒随气流进入导气管;氧气不易溶于水且不和水发生化学反应;
K2MnO4+MnO2+O2↑;防止高锰酸钾颗粒随气流进入导气管;氧气不易溶于水且不和水发生化学反应;