
| A. | 该反应是置换反应 | B. | 图中气体单质的化学式为H2 | ||
| C. | 反应后原子的个数减少 | D. | 水煤气泄漏会污染空气 |
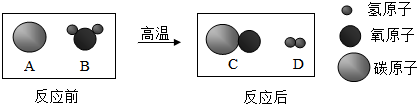
分析 观察工业生产水煤气的化学反应微观示意图,根据反应的特点分析反应的类型;根据微粒的构成写出化学式;根据微粒的变化分析分子、原子等的变化;一氧化碳是有毒的气体,能污染空气.据此分析判断有关的问题.
解答 解:A、由工业生产水煤气的化学反应微观示意图可知,该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,故A正确;
B、由微粒的构成可知,图中气体单质的化学式为H2,故B正确;
C、由微粒的变化可知,反应后原子的个数不变,故C错误;
D、水煤气的成分中含有一氧化碳,一氧化碳是有毒的气体,水煤气泄漏会污染空气.故D正确.
故选C.
点评 化学反应的实质是分子破裂为原子,原子重新组成新的分子,化学变化前后原子的种类、数目不变,分子的种类一定改变.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
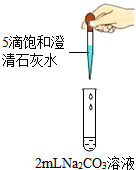 学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊.甲组同学进行如图1所示的实验,却未观察到预期现象.
学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊.甲组同学进行如图1所示的实验,却未观察到预期现象.| 实验目的 | 实验操作 | 实验现象 | |
| 探究猜想② | 取4支试管,向其中分别加入… | 碳酸钠溶液浓度/% | 是否浑浊 |
| 10 | 不浑浊 | ||
| 5 | 不浑浊 | ||
| 1 | 浑浊 | ||
| 0.5 | 浑浊 | ||

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
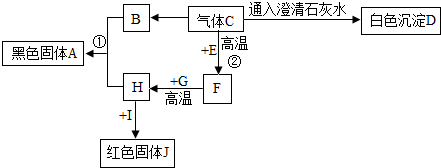
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
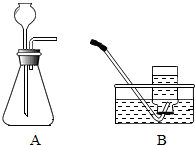 某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象,硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象,硫酸中混有硫酸铜溶液时,产生氢气的速率更快.| 编号 | 20%的硫酸各20ml | 锌粒 | 收集1瓶氢气所需的时间 |
| ① | 加入质量分数为10%的硫酸铜溶液1ml | 1g | 2分10秒 |
| ② | 加入质量分数为10%的硫酸锌溶液1ml | 1g | 3分01秒 |
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | 取1g锌粒于锥形瓶中,加入20ml20%的稀硫酸 | ②中反应速率比①快 | 产生氢气的速率较快与铜单质有关 |
| ② | 取1g锌粒于锥形瓶,加入少量铜,再加入20mL20%的稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ti可以表示一个钛原子 | B. | Ti4+核外有26个电子 | ||
| C. | TiO2中含有氧分子 | D. | CaTiO3属于金属氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
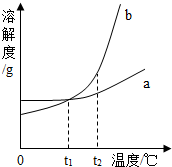 如图是a、b两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
如图是a、b两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | t2℃时,a溶液的溶质质量分数一定小于b溶液的溶质质量分数 | |
| B. | t1℃时,a、b两种物质的饱和溶液溶质质量分数相同 | |
| C. | 将t2℃时b的不饱和溶液降温至t1℃,一定能得到b的饱和溶液 | |
| D. | 若a中混有少量的b,可以用降温结晶的方法提纯a |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com