
在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码
D.用了含少量杂质的蔗糖配制溶液
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
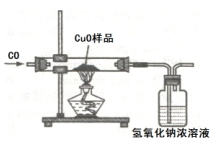 金属的冶炼时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数,实验所取氧化铜样品质量为10克.(所含杂质不参加反应)
金属的冶炼时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数,实验所取氧化铜样品质量为10克.(所含杂质不参加反应)查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 甲 | 乙 | 丙 | 丁 | |
| 加入氢氧化钠溶液质量(g) | 10.0 | 20.0 | 40.0 | 60.0 |
| 反应得到沉淀的质量(g) | 1.45 | 2.9 | 5.8 | 5.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源:【全国区级联考】江苏省盐城市亭湖区2017届九年级毕业班下学期第二次质量检测化学试卷 题型:选择填充题
甲和乙可以合成清洁燃料丙,微观过程如图。下列说法错误的是

A. 甲中碳元素的化合价为+2价 B. 丙中C、H、O的质量比为12:3:8
C. 丁的化学式为H2O2 D. 该反应体现无机物可转化为有机物
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 减少空气中可吸入颗粒物的含量 | B. | 缓和温室效应 | ||
| C. | 减少酸雨的发生 | D. | 防止臭氧层空洞进一步扩大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com