
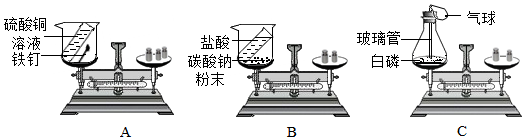
分析 (1)根据硫酸铜溶液与铁钉反应生成硫酸亚铁和铜,写出反应的方程式解答;
(2)根据用实验来验证质量守恒定律,那么结果不外乎两个:相等(当没有气体参加或不生成气体时)、不相等 (当有气体参加或生成气体时)解答;
(3)根据白磷燃烧的现象及化学方程式的书写步骤解答.
解答 解:(1)①硫酸铜溶液与铁钉反应生成硫酸亚铁和铜,烧杯内反应的实验现象为铁钉表面出现红色的固体,溶液有蓝色变为浅绿色;
②甲同学所做的实验中,没有气体参加或生成,所以左右肯定平衡,故选C;
(2)①乙同学所做的实验中,盐酸与碳酸钠粉末反应生成氯化钠和水和二氧化碳,有气体二氧化碳生成,故造成天平的指针向右偏转,该反应符合质量守恒定律;
②要想使两边相等,只能把生成的气体收集起来,不让其出去,也就是说必须在密闭容器中进行了;
③质量守恒的原因:微观是因为:在化学反应前后,原子的种类、原子的数目、原子的质量不变,故在化学反应前后总质量不变;
(3)白磷燃烧放出热量,温度升高,导致气球膨胀,反应后冷却至室温后,由于锥形瓶中的氧气消耗,压强减小,气球变瘪,因此气球发生的变化是先变大后变小;
该反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故答案为:(1)①铁钉表面出现红色的固体,溶液有蓝色变为浅绿色;②C;
(2)①符合;
②在密闭容器中进行;
③在化学反应前后,原子的种类、原子的数目、原子的质量不变;
(3)先变大后变小;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
点评 本题考查的是质量守恒定律的运用,理解微观上质量守恒的原因、注意反应物或生成物中气体易被忽略等是正确解答本题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题

| A. | 该反应中H2S被氧化 | |
| B. | 反应前后各元素的化合价均不变 | |
| C. | 化学反应前后分子个数保持不变 | |
| D. | 参加反应的两种分子的个数比为4:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是关于碳和碳的氧化物的知识网络图(图中“→”表示转化关系,“…”表示相互能反应),下列说法正确的是( )
如图是关于碳和碳的氧化物的知识网络图(图中“→”表示转化关系,“…”表示相互能反应),下列说法正确的是( )| A. | “CO2→CaCO3”的反应可用于检验二氧化碳 | |
| B. | “CO→CO2”的反应类型为置换反应 | |
| C. | “C …CO2”的反应是放热反应 | |
| D. | “CO2?H2CO3”的反应可用酚酞试剂验证 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 500 g | B. | 100 g | C. | 200 g | D. | 400 g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
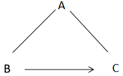
| A. | A是无色气体,B、C为常见金属单质 | |
| B. | A、B均为黑色固体,B、C均为氧化物 | |
| C. | A为黑色固体单质,B、C为元素组成相同的氧化物 | |
| D. | A是非金属固体单质,B、C是气体,B与光合作用息息相关 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
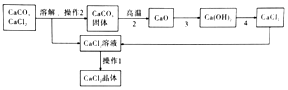
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

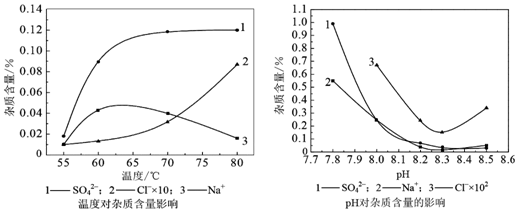

| 装置C/g | 装置D/g | 装置E/g | |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com