
科目:初中化学 来源: 题型:选择题
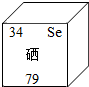 硒是人体必需的微量元素之一,具有抗癌,保护心肌等需要功能.缺硒时,机体免疫功能降低,容易发生癌症和其他疾病.硒在元素周期表中的信息如图,有关硒的说法不正确的是( )
硒是人体必需的微量元素之一,具有抗癌,保护心肌等需要功能.缺硒时,机体免疫功能降低,容易发生癌症和其他疾病.硒在元素周期表中的信息如图,有关硒的说法不正确的是( )| A. | 硒元素是非金属元素 | B. | 硒的元素符号是Se | ||
| C. | 硒元素的原子核外电子数为79 | D. | 硒元素的相对原子量为79 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4Fe+3O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3 | B. | NaOH+CO2═Na2CO3+H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A. | 该变化的基本反应类型是化合反应 | B. | 反应后物质M的质量为13 g | ||
| C. | 反应中N、P的质量比为4:5 | D. | 物质Q可能是该反应的催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 海水中的水发生了燃烧 | B. | 海水中的盐发生了燃烧 | ||
| C. | 海水中的水分解产生氢气发生燃烧 | D. | 海水中可能溶解了某种有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
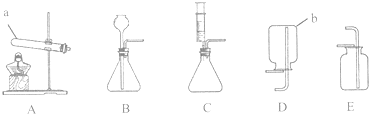
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
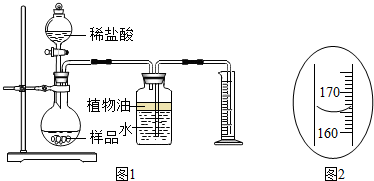 为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.
为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动.| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液 | 溶液变成红色 | 该样品还含有氢氧化钙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com