下列各物质都含有少量杂质(括号内为杂质)写出除去杂质的主要操作及有关化学方程式
(1)CuO(Cu) .
(2)CaO(CaCO3) .
(3)NaCl(Na2CO3) .
(4)FeSO4(CuSO4) .
【答案】
分析:分析各组内物质的性质差异,选择所给的物质与杂质反应而除去,并且不生成新的杂质.铜受热后能生成氧化铜,碳酸钙高温分解生成氧化钙,碳酸钠和盐酸反应生成氯化钠,铁和硫酸铜反应生成硫酸亚铁.
解答:解:(1)铜在氧气中加热生成氧化铜,故可以在氧气流中加热混合物,化学方程式为:2Cu+O
2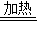
2CuO;
(2)氧化钙中混有的碳酸钙高温可以分解为氧化钙,CaCO
3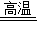
CaO+CO
2↑.
(3)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳.通过该反应可以将碳酸钠转化为氯化钠.
该反应的化学方程式为:Na
2CO
3+2HCl═2NaCl+H
2O+CO
2↑.
(4)除去FeSO
4中CuSO
4,根据铁能置换出硫酸铜的铜,可加入足量的铁粉后过滤,化学方程式为:Fe+CuSO
4=FeSO
4+Cu.
故答案为:(1)在氧气流中灼烧;2Cu+O
2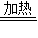
2CuO.
(2)高温煅烧; CaCO
3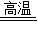
CaO+CO
2↑.
(3)加稀盐酸后蒸发;Na
2CO
3+2HCl═2NaCl+H
2O+CO
2↑.
(4)加入足量的铁粉后过滤; Fe+CuSO
4=FeSO
4+Cu.
点评:解答本题时要充分理解物质的性质及其书写化学方程式的方法,只有这样才能对问题做出正确的判断.

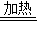 2CuO;
2CuO;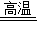 CaO+CO2↑.
CaO+CO2↑.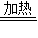 2CuO.
2CuO.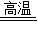 CaO+CO2↑.
CaO+CO2↑.
