

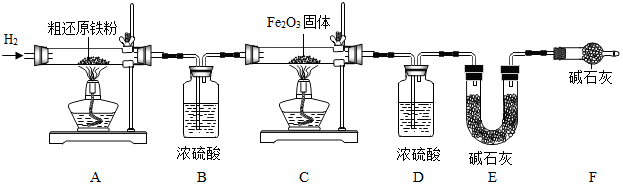
分析 (1)氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳;
(2)步骤⑥的目的是 防止生成的还原铁粉再次被氧化,起保护作用;
(3)若缺少装置D,不影响测氧元素的质量分数;实验后,甲同学根据装置E的增重算得样品中碳元素的质量分数.
解答 解:(1)氧化铁在高温条件下能与CO发生反应生成铁与二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;故填:Fe2O3+3CO$\frac{\underline{\;点燃\;}}{\;}$2Fe+3CO2.
(2)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃C处酒精灯;
④点燃A 处酒精灯;
⑤分别熄灭A、C处酒精灯;
⑥继续通H2直至装置冷却;
⑦再次称量必要装置的质量.步骤⑥的目的是防止生成的还原铁粉再次被氧化,起保护作用.
故填:继续通H2直至装置冷却;防止生成的还原铁粉再次被氧化.
(3)若缺少装置D,则所测氧元素的质量分数将不变,这是因为需要的水的质量数据是从B装置得到的.
装置E增重m3,则甲烷与氧化铁反应生成二氧化碳的质量为m3,生成二氧化碳中碳元素质量=m3×$\frac{12}{44}$=$\frac{3}{11}$m3;样品中碳元素的质量分数=$\frac{\frac{3}{11}{m}_{3}}{M}$×100%=$\frac{3{m}_{3}}{11M}$×100%.
故填:不变;$\frac{3{m}_{3}}{11M}$×100%.
点评 通过对铁冶炼原理的知识迁移,理解该题的实验过程及目的,考查了知识的运用及实验分析的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
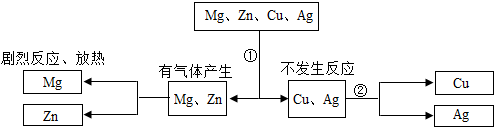 某同学为探究镁、锌、铜、银的活动性顺序,设计如图实验流程:依据流程设计,下面对物质①②的选择合理的是( )
某同学为探究镁、锌、铜、银的活动性顺序,设计如图实验流程:依据流程设计,下面对物质①②的选择合理的是( )| A. | ①稀硫酸②硝酸银 | B. | ①稀盐酸②硫酸锌 | ||
| C. | ①稀盐酸②硫酸亚铁 | D. | ①稀硫酸②氯化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”表示有可循环利用的物质)
”表示有可循环利用的物质)
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
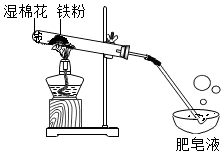 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸. | 若固体不溶解,也没有气泡冒出,剩余固体是Fe3O4.若固体部分溶解,有气泡冒出,剩余固体是Fe与Fe3O4. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 物质 | 性质 | 用途 |
| A | 一氧化碳 | 还原性 | 冶炼金属 |
| B | 氧气 | 助燃性 | 医疗急救 |
| C | 活性炭 | 吸附性 | 防毒面具 |
| D | 干冰 | 蒸发时吸收热量 | 制冷剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com