
分析 根据已有的知识进行分析解答,甲醇燃烧生成二氧化碳和水,根据物质的检验方法进行分析解答,根据化学式的差别确定物质的类别.
解答 解:(1)甲醇燃烧生成二氧化碳和水,故填:2CH3OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$ 2CO2+4H2O;
(2)甲醇燃烧生成二氧化碳可以使用澄清的石灰水检验,故填:澄清石灰水;
(3)在甲醇和乙醇中,碳氢元素的质量比不同,故可以通过从测定的二氧化碳和水的质量,计算出碳氢元素的质量比,从而将甲醇和乙醇分开,故填:碳、氢元素的质量比.
点评 本题考查的是常见的可燃物的性质,完成此题,可以依据已有的物质的性质进行.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:多选题
| A. | 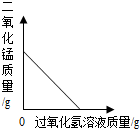 向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. | 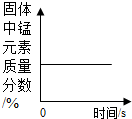 加热一定量的高锰酸钾固体 | |
| C. | 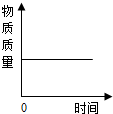 镁带在耐高温的密闭容器(内含空气)内加热, | |
| D. | 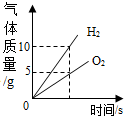 将水通电电解一段时间 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 气割时,纯铁板的质量一定等于气割后两块铁板和铁渣的质量和 | |
| B. | 10g高锰酸钾充分分解后,所得剩余固体的质量一定为10g | |
| C. | 3g 碳和8g 氧气充分反应,生成11g 二氧化碳 | |
| D. | 100g 固体二氧化碳(俗称“干冰”) 升华后变成100g 二氧化碳气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
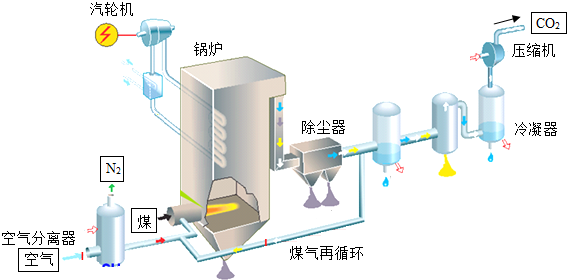
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 用足量稀盐酸溶解后过滤,并洗净和干燥所得固体 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | NH3 | 通过浓硫酸洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
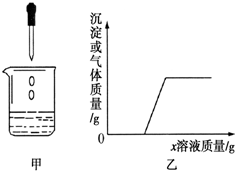 向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是A
向烧杯中逐滴加入x溶液至过量(图甲),生成沉淀或气体的质量与加入x溶液的质量关系符合图乙的是A| 烧杯中的物质 | x溶液 | |
| A | 稀盐酸和硫酸铜溶液 | 烧碱溶液 |
| B | 稀硫酸和稀盐酸 | 氯化钡溶液 |
| C | 镁铝合金 | 稀盐酸 |
| D | 氢氧化钠和碳酸氢钠溶液 | 稀盐酸等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 分析及结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com