
分析 (1)含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥,据此进行分析解答.
(2)测定溶液酸碱性,可选用酸碱指示剂,结合石蕊溶液遇酸性溶液变红色,酚酞溶液遇酸性溶液不变色,进行分析解答即可.
(3)生石灰能与稀硫酸反应生成硫酸钙和水,进行分析解答.
解答 解:(1)A、K2CO3中含有钾元素,属于钾肥.
B、(NH4)2SO4中含有氮元素,属于氮肥.
C、磷矿粉中含有磷元素,属于磷肥.
D、CO(NH2)2中含有氮元素,属于氮肥.
(2)石蕊溶液遇酸性溶液变红色,酚酞溶液遇酸性溶液不变色,故测定土壤的酸性,可选用实验室中的紫色石蕊溶液;紫色玫瑰花的汁液遇酸性溶液变红,故可代替紫色石蕊溶液测定土壤呈酸性.
(3)生石灰与稀硫酸反应生成硫酸钙和水,反应的化学方程式为:CaO+H2SO4=CaSO4+H2O.
故答案为:(1)BD;(2)紫色石蕊溶液;(3)CaO+H2SO4=CaSO4+H2O.
点评 本题难度不大,了解化肥的分类方法、常见酸碱指示剂的性质、酸的化学性质是正确解答本题的关键.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 目的 | 操作 | 现象 | 结论 |
| A | 比较铝和铜的金属活动性 | 将砂纸打磨过的铝丝 浸入到硫酸铜溶液中 | 铝丝表面有红色固体析出 | 铝比铜活泼 |
| B | 检验盐酸和氢氧化钠溶液是否恰好完全反应 | 在反应后的无色溶液中滴加无色的酚酞试液 | 无明显现象 | 恰好完全反应 |
| C | 探究物质溶解于 水时的热量变化 | 向一定量水中加入硝酸铵晶体,充分搅拌 | 溶液温度下降 | 盐类物质溶解于水时,都会吸热 |
| D | 检验集气瓶中是否集满二氧化碳 | 将燃着的木条伸入集 气瓶中 | 木条火焰熄灭 | 集气瓶中已集满二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
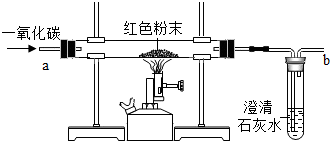 在实验探究课上,老师给同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请回答下列问题.
在实验探究课上,老师给同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请回答下列问题.| 实验中可能出现的现象 | 结论 |
| 红色粉末不变色,石灰水不变浑浊 | 猜想1成立 |
| 红色粉末全部变为黑色,石灰水变浑浊 | 猜想2成立 |
| 红色粉末部分变为黑色,石灰水变浑浊 | 猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 甲、乙、丙是三种常见的物质,它们之间的相互转化关系如右图所示,”→“表示由一种物质转化为另一种物质(图中部分反应条件及物质略去).
甲、乙、丙是三种常见的物质,它们之间的相互转化关系如右图所示,”→“表示由一种物质转化为另一种物质(图中部分反应条件及物质略去).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 因为通常CO2的密度大于空气的密度,故可用向上排空法收集 | |
| B. | 在发生装置中加入块状石灰石和稀硫酸 | |
| C. | 因为CaCO3与稀盐酸在常温下即可反应,故气体发生装置不需加热 | |
| D. | 盛满CO2的集气瓶,盖上瓶盖,正放在桌面上 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
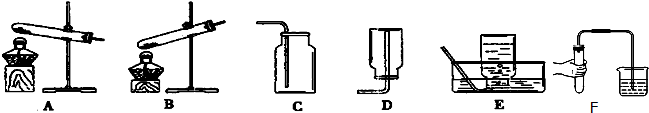
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 90% | B. | 80% | C. | 76% | D. | 72% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
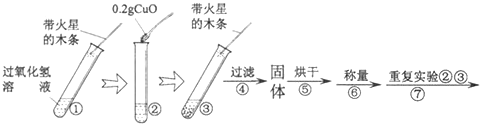
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出 带火星的木条复燃 | 称量CuO的质量仍为0.2g | 溶液中有大量气泡放出,带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立猜想Ⅲ成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com