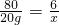铝跟盐酸或氢氧化钠溶液都能反应,且都有氢气产生.反应的化学方程式分别可表示如下:2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(1)相同条件下等质量的铝分别跟足量的盐酸、氢氧化钠溶液完全反应,放出氢气的质量关系是________(填序号).
A、铝跟盐酸反应放出的氢气多 B、铝跟氢氧化钠溶液反应放出的氢气多
C、反应放出氢气一样多 D、不能判断
(2)20g氢氧化钠固体溶于水,可配制质量分数为10%的氢氧化钠溶液________g.
(3)用上述NaOH溶液和足量的铝反应,可以制取H2多少克?
解:(1)根据题意和反应的化学方程式:2Al+6HCl=2AlCl
3+3H
2↑;2Al+2NaOH+2H
2O=2NaAlO
2+3H
2↑进行分析,反应的铝与生成氢气的分子个数比较可知生成氢气相等.故选C;
(2)由题意根据溶液的溶质质量分数计算方法得溶液质量:20g÷10%=200g
(3)解:设可制得氢气的质量为x
2Al+2NaOH+2H
2O=2NaAlO
2+3H
2↑
80 6
20g x
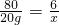
x=1.5g
答:可制得氢气的质量为1.5g.
故答案为:(1)C;(2)200g;(3)1.5g.
分析:(1)根据根据化学方程式,找出各物质间的比,列出比例式,就可计算出铝的质量;
(2)根据溶液的溶质质量分数计算公式计算;
(3)根据铝跟盐酸或氢氧化钠溶液都能发生反应生成氢气的化学方程式即可看出生成氢气的多少.
点评:本题主要考查学生对参加反应的物质质量数的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.