
分析 (1)化学式中各元素的质量比为各元素的相对原子质量×原子个数的之比,据此分析计算回答.
(2)将浓盐酸稀释为稀盐酸的步骤是;计算、量取、稀释、装瓶;
(3)可先根据化学方程式求出氢氧化钠的质量,再根据废水中氢氧化钠的质量分数求出废水的质量.
解答 解:
(1)根据纤维素的化学式(C6H1005)n知,纤维素中C、H、O三种元素的质量比=(12×6):(1×10):(16×5)=36:5:40.
(2)用质量分数为37%的浓盐酸配制质量分数为10%的稀盐酸100g,配制的步骤依次为计算需要浓盐酸的质量、进而计算其体积,然后用量筒量取浓盐酸、水,并混合稀释溶解,装瓶;
(3)196g废硫酸溶液中含硫酸的质量为196g×20%=3920g
设196g废硫酸溶液可以反应氢氧化钠的质量为x
H2SO4 +2NaOH=Na2SO4 +2H2O
98 80
3920g x
$\frac{98}{80}$=$\frac{3920g}{x}$
x=320g
则需要氢氧化钠的废水的质量=$\frac{320g}{1.6%}$=2000g
故答案为:
(1)36:5:40;(2)量取;稀释;(3)答:可以处理的废水质量是2000g.
点评 本题主要考查化学式的含义、溶液配制及根据化学方程式进行简单计算的能力.难度不大,根据已有的知识即可分析解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
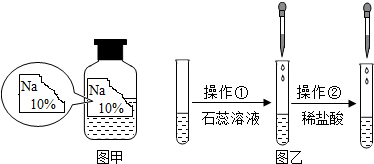 某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
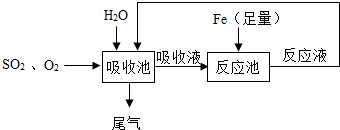 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验序号 | 实验1 | 实验2 | 实验3 | 实验4 |
| 水的质量 | 100g | 100g | 100g | 100g |
| 加入物质质量 | 98%的浓硫酸5g | 氧化钠5g | 硫酸铜晶体5g | 碳酸钠5g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
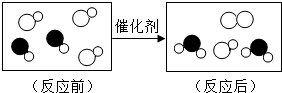 化学与生活、生产密切相关,请用所学的知识下列填空
化学与生活、生产密切相关,请用所学的知识下列填空查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用氢氧化钠溶液清洗盛装过植物油的瓶子 | |
| B. | 用酒精或汽油清洗掉衣服上的油污 | |
| C. | 用稀盐酸清洗盛装过石灰水的试剂瓶 | |
| D. | 加了餐具洗洁精的热水洗涤碗碟上的油污 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com