
| A. | CH3COCH3 | B. | CH3COOH | C. | CH4 | D. | C |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 在“2H3PO4”化学符号中的,“1”表示一个磷元素 | |
| B. | 在“2H3PO4”化学符号中的,“2”表示两个H3PO4分子 | |
| C. | 在“2H3PO4”化学符号中的,“3”表示每个H3PO4分子含有三个氢原子 | |
| D. | 在“2H3PO4”化学符号中的,“4”表示每个H3PO4分子含有四个氧原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
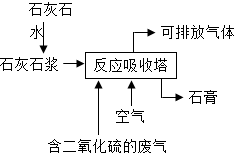 工业用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要 成分为硫酸钙).简易流程如图,主要的反应为:2CaCO3+2SO2+O2═2CaSO4+2X.
工业用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要 成分为硫酸钙).简易流程如图,主要的反应为:2CaCO3+2SO2+O2═2CaSO4+2X.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 我国首架C919大飞机下线,标志着我国跻身飞机研制先进国家行列.
我国首架C919大飞机下线,标志着我国跻身飞机研制先进国家行列.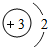 ,该粒子是C.
,该粒子是C.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com