
分析 物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.食醋、牛奶、加碘盐、水中,水属于纯净物,其它的属于混合物;冰、干冰、氧化铁、铜绿中,铜绿属于混合物,其它属于氧化物;蛋白质、油脂、维生素、煤气中,蛋白质、油脂、维生素属于有机物,煤气不是;纯碱、烧碱、熟石灰、氢氧化镁中,纯碱属于盐,其它属于碱.
解答 解:食醋、牛奶、加碘盐、水中,水属于纯净物,其它的属于混合物;冰、干冰、氧化铁、铜绿中,铜绿属于混合物,其它属于氧化物;蛋白质、油脂、维生素、煤气中,蛋白质、油脂、维生素属于有机物,煤气不是;纯碱、烧碱、熟石灰、氢氧化镁中,纯碱属于盐,其它属于碱;故答案为:水;铜绿;煤气;纯碱;
点评 本考点考查了物质的分类,要加强记忆有关的知识点,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
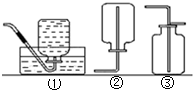 通常状况下,氢气是一种无色无味的气体,密度比空气小,难溶于水.如图所示的三种气体收集方法中,适宜收集氢气的方法有( )
通常状况下,氢气是一种无色无味的气体,密度比空气小,难溶于水.如图所示的三种气体收集方法中,适宜收集氢气的方法有( )| A. | ①②③ | B. | ②③ | C. | ①③ | D. | ①② |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 (1)小明用如图所示装置探究可燃物燃烧的条件.他发现热水中的白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷和水中的白磷都不燃烧.请回答:
(1)小明用如图所示装置探究可燃物燃烧的条件.他发现热水中的白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷和水中的白磷都不燃烧.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
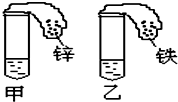 如图所示,在试管和小气球中分别先加入浓度、质量均相等的足量稀硫酸和等质量的金属锌、铁,然后将气球中的金属倒入试管中,观察到的现象是:试管中有气泡产生,开始时,甲气球迅速鼓起,而乙气球鼓起较慢;反应结束后,甲气球体积比乙气球小(填:大、小、一样大)
如图所示,在试管和小气球中分别先加入浓度、质量均相等的足量稀硫酸和等质量的金属锌、铁,然后将气球中的金属倒入试管中,观察到的现象是:试管中有气泡产生,开始时,甲气球迅速鼓起,而乙气球鼓起较慢;反应结束后,甲气球体积比乙气球小(填:大、小、一样大)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
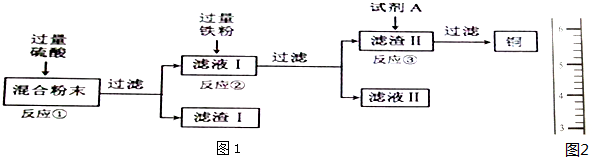
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com