(2013?大庆)现有一定质量含有少量泥沙等不溶性杂质和少量Na
2SO
4,MgCl
2,CaCl
2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下:
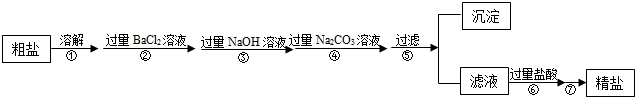
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为
蒸发结晶
蒸发结晶
.
(2)请写出实验步骤②中所涉及的化学方程式
BaCl2+Na2SO4═BaSO4↓+2NaCl
BaCl2+Na2SO4═BaSO4↓+2NaCl
.
(3)步骤⑥中加入过量盐酸的目的是
除去过量的氢氧化钠和碳酸钠
除去过量的氢氧化钠和碳酸钠
.
(4)步骤②和步骤④
不可以
不可以
(填“可以”或“不可以”)颠倒,理由是
如果颠倒,无法除去过量的氯化钡
如果颠倒,无法除去过量的氯化钡
.
(5)检验步骤④中Na
2CO
3溶液已过量的方法是
取上层清液于试管中,滴加氯化钙溶液,如果出现白色沉淀,说明碳酸钠溶液已经过量
取上层清液于试管中,滴加氯化钙溶液,如果出现白色沉淀,说明碳酸钠溶液已经过量
.
(6)加碘食盐相关信息如图所示.
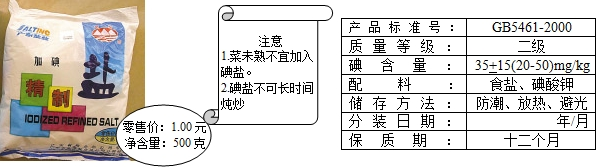
食盐中的碘酸钾(KIO
3)在酸性条件下,可以将碘化钾(KI)变成碘(I
2),化学方程式如下:
KIO
3+5KI+6HCl=6KCI+3I
2+3H
2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象
混合液由无色变成蓝色
混合液由无色变成蓝色
.
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na
2S
2O
3),发生化学反应方程式为:2Na
2S
2O
3+I
2═Na
2S
4O
6+2NaI
当加入质量分数为0.237%Na
2S
2O
3溶液2g时,I
2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na
2S
2O
3的相对分子质量为158.请写出计算过程).

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
