
铁、铜是我们生活中常见的金属。
(1)下列生活用品中,铁锅用来做饭是利用了铁的 性,铜丝作导线是利用了铜的 性。

(2)根据右侧转化关系图,回答问题。
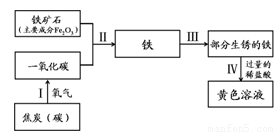
①铁生锈的条件是 。
②写出步骤II中的化学方程式 。
③黄色溶液中的溶质是 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:2012年河南省中招临考猜题化学试卷(四)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com