

| ||
| ||
| 160 |
| x |
| 48 |
| 10g-7.6g |
| 8g |
| 10g |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
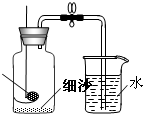 在”空气中氧气含量的测定”实验探究中,小明进行如下实验:将红磷盛放在燃烧匙中,点燃后立即插入集气瓶内并塞上瓶塞.
在”空气中氧气含量的测定”实验探究中,小明进行如下实验:将红磷盛放在燃烧匙中,点燃后立即插入集气瓶内并塞上瓶塞.查看答案和解析>>
科目:初中化学 来源: 题型:
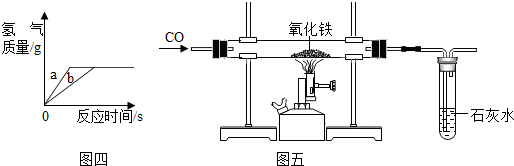
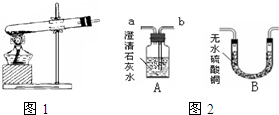 2010年5月18日是第34个国际博物馆日,我省对大冶铜绿山古铜矿遗址博物馆进行了全面修缮,并将外墙全部改为铜绿色,该馆现以全新姿容开门迎宾.已知铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.红星中学一化学兴趣小组通过实验探究,分析黑色固体的组成,并验证产生的气体.请你参与探究活动:
2010年5月18日是第34个国际博物馆日,我省对大冶铜绿山古铜矿遗址博物馆进行了全面修缮,并将外墙全部改为铜绿色,该馆现以全新姿容开门迎宾.已知铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.红星中学一化学兴趣小组通过实验探究,分析黑色固体的组成,并验证产生的气体.请你参与探究活动:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com