
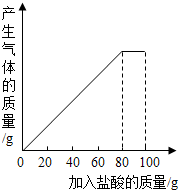
 课外小组同学将100g盐酸分5次加入到35g某石灰石样品中(已知杂质不与盐酸反应),得到如表部分数据和如图图象.(最后结果保留一位小数)
课外小组同学将100g盐酸分5次加入到35g某石灰石样品中(已知杂质不与盐酸反应),得到如表部分数据和如图图象.(最后结果保留一位小数)| 次数 | 1 | 2 | 3 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
分析 (1)根据反应的图象可知,在加入80g稀盐酸即第4次加入后,恰好反应完全,此后再加稀盐酸也不再会反应放出二氧化碳了,因此,前四次实验固体都得到充分反应;
根据第1次反应的数据可推知每加入20g稀盐酸,充分反应后,剩余固体减少的质量,据此规律可推断a值;
(2)4次反应固体物质减少的质量即为样品中碳酸钙的质量,据此计算生成二氧化碳的质量即可;
(3)利用第四次反应恰好反应完全以及方程式可以计算反应的氯化氢的质量,进而计算盐酸的溶质质量分数
解答 解:(1)由第一次加入20g稀盐酸固体质量将会减少35g-30g=5g,所以结合图象中的信息可知:第2次加入20g稀盐酸后,所剩余固体的质量=30g-5g=25g;
(2)由图象可知在加入80g稀盐酸即第4次加入后,恰好反应完全,故第4次加入稀盐酸后,固体物质总共减少的质量=5g×4=20g,及样品中碳酸钙的质量是20g
设20g碳酸钙完全反应生成二氧化碳质量为x,反应的氯化氢质量是y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
20g y x
$\frac{100}{20g}=\frac{73}{y}=\frac{44}{x}$x=8.8g y=14.6g
(3)稀盐酸中溶质的质量分数为$\frac{14.6g}{80g}$×100%=18.3%
故答案为:(1)25;(2)该石灰石样品可制取二氧化碳的质量是8.8g.(3)稀盐酸中溶质的质量分数为18.3%.
点评 把握住记录数据中在发生着变化的数据,分析数据变化的原因或变化的规律,这是分析实验数据的一种常用方法,也是这类题的解题关键.


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源:2017届上海市杨浦区九年级4月学业质量调研化学试卷(解析版) 题型:选择填充题
化学用语的表述正确的是
A. 2O—两个氧元素 B. 2N2—2个氮分子
C. FeSO4—表示硫酸铁 D. C60—60个碳原子
查看答案和解析>>
科目:初中化学 来源:2017届湖南省张家界市永定区九年级下学期期中考试(一模)化学试卷(解析版) 题型:选择题
人们在阳光照射的树林里,会感到空气特别的清新,其原因就是树林里有极少部分的氧气被转化成具有杀菌消毒作用的臭氧(O3).下列关于臭氧和氧气的说法正确的是
A.它们属于氧化物
B.它们都是由氧元素组成
C.它们同属于一种物质
D.它们的物理性质和化学性质完全相同
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl、Ba(OH)2、Mg(NO3)2 | B. | NaCl、Fe(OH)3、Ba(NO3)2 | ||
| C. | Na2SO4、MgCl2、Cu(NO3)2 | D. | H2SO4、KOH、NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
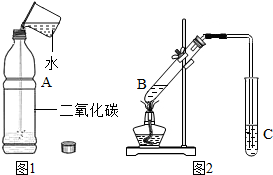 二氧化碳是导致温室效应的主要原因之一,空气中二氧化碳的增加,主要来 源于化石燃料的燃烧,所以人们一方面想限制其排放量,另一方面又想对它进行再利用.
二氧化碳是导致温室效应的主要原因之一,空气中二氧化碳的增加,主要来 源于化石燃料的燃烧,所以人们一方面想限制其排放量,另一方面又想对它进行再利用.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
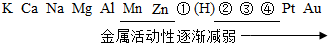
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲>乙>铜 | B. | 甲>铜>乙 | C. | 乙>铜>甲 | D. | 铜>甲>乙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com