
【题目】(8分)为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
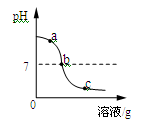
(1)由图可知该实验操作是将 滴加到另一种溶液中;
(2)该反应的化学方程式为 ;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现 的现象。结论:该样品是a处溶液。
②为进一步确定b或c处溶液,又设计了以下方案:
实验步骤 | 实验现象 | 实验结论 |
另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液。 | 该样品为b处溶液。 | |
该样品为c处溶液,并推知溶液中的阳离子有 。 |
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑 。
【答案】(1)稀盐酸 (2) Ca(OH)2+2HCl==CaCl2+2H2O
(3)【探究过程】①溶液由无色变成红色
②
实验步骤 | 实验现象 | 结论 |
只产生白色沉淀(产生白色沉淀也可) | ||
先产生气泡,后产生白色沉淀 | 该样品为c处溶液,并推知溶液中的阳离子有Ca2+ 、H+ |
【反思评价】 反应物是否过量
【解析】
试题分析:由图可知该实验操作是将稀盐酸滴加到氢氧化钙中,因为开始时溶液的PH值大于7,该反应的化学方程式为Ca(OH)2+2HCl==CaCl2+2H2O;该样品是a处溶液属于碱性因此溶液由无色变成红色;为进一步确定b或c处溶液
实验步骤 | 实验现象 | 结论 |
只产生白色沉淀(产生白色沉淀也可) | ||
先产生气泡,后产生白色沉淀 | Ca2+ 、H+ |
从该实验看出:探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑反应物是否过量。


科目:初中化学 来源: 题型:
【题目】在pH=2的溶液中,下列离子能大量共存,且溶液为无色的是( )
A.K+、OH﹣、NO3﹣ B.NH4+、Cu2+、Cl﹣
C.Ca2+、CO32﹣、Cl﹣ D.K+、Na+、SO42﹣
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答:
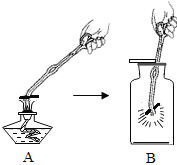
(1)A图中,用坩埚钳夹取一小块木炭在酒精灯火焰的 部分迅速加热;从燃烧条件的角度分析,加热的目的是 。
(2)B图中,燃烧停止后,取出坩埚钳,往集气瓶里加入少量的澄清石灰水并振荡,观察到的现象是 ,发生反应的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】盐城濒临黄海,海盐文化全国知名.某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究:
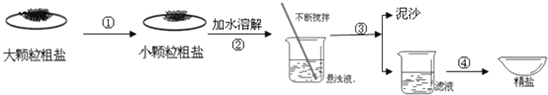
(1)操作①中必须用到的一种仪器是 (填序号)
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作③的名称是 ,操作④中用到玻璃棒,作用为 .
(3)用提纯得到的“精盐”配制100g 7.5%的氯化钠溶液.经检测,溶质质量分数偏小,其原因可能有 (填序号)
①氯化钠固体不纯
②称量时精盐与砝码放反了
③量取水时俯视读数
④装瓶时,有少量溶液洒出
(4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如下处理:

①白色沉淀的化学式为 .
②在得到的滤液中加入足量的稀盐酸的目的是 .
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将 (填“大于”、“小于”或“等于”)原精盐中NaCl的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“一定溶质质量分数的氯化钠溶液的配制”两个实验。
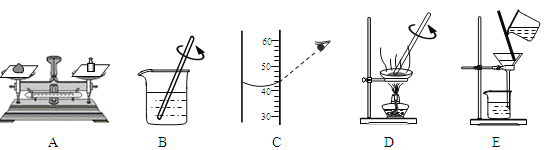
(1)操作E中得到的滤液仍浑浊,其原因可能是 (答出一点即可);
(2)若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会 (填“偏大”、“偏小”或“不变”);
(3)图D中玻璃棒的作用是 ;
(4)图C中有一处明显的错误,请你改正: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
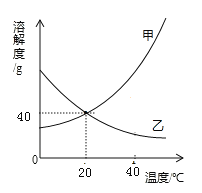
【题目】物质甲、乙的溶解度随温度变化图象如图所示,根据如图回答问题:
(1)由图你能获得哪些信息
① ;② 。
(2)20℃时,将50克甲溶于100克水中,所得溶液为 溶液(填“饱和”、“不饱和”溶液)。
(3)40℃时,甲、乙两种物质的溶解度大小关系:甲 乙(填“>”、“<”或“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】建立基本的化学观念可以让我们更好的理解化学,如形成守恒观念,可以更好的理解质量守恒定律,下列表述正确的是
A.每1个C原子和1个O2分子反应,生成2个CO2分子
B.32g S与32g O2完全反应,生成64g SO2
C.镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律
D.根据:蜡烛+氧气![]() 二氧化碳+水,则蜡烛中一定含有C、H、O三种元素
二氧化碳+水,则蜡烛中一定含有C、H、O三种元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的第二杀手﹣﹣心脑血管疾病,这类疾病患者大多数属于酸性体质,应经常食用碱性食品.根据下表的信息,这类患者应经常食用的食物为( )
食物 | 葡萄 | 牛奶 | 豆制品 | 苹果 |
pH | 3.5~4.5 | 6.3~7.3 | 7.4~7.9 | 2.9~3.3 |
A.牛奶 B.葡萄 C.苹果 D.豆制品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com