
【题目】已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4)。相关反应的化学方程式为:CaC2O4+2HCl=CaCl2+H2C2O4
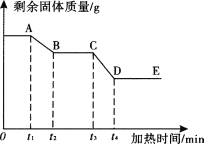
(1)实验一:取一定量草酸钙固体,加热。加热过程中剩余固体的质量随时间变化如右图所示。图中AB段发生反应的化学方程式为_______________________,DE段固体所含物质为________(写化学式或物质名称均可,下同)。
(2)实验二:探究草酸钙加热一段时间后剩余固体M的成分。

(3)若加热前草酸钙的质量为6.4g,加热一段时间后剩余固体的质量为4.8g,则该固体中含有的物质是______________________。
【答案】(1)CaCO3高温CaO+CO2↑;CaO(2)白色固体产生;无;CaCO3;CaC2O4(3)CaCO3;CaO
【解析】
试题分析:取一定量草酸钙固体,加热。加热过程中剩余固体的质量随时间变化如右图所示。图中AB段发生反应的化学方程式为CaCO3高温CaO+CO2↑,DE段固体所含物质为CaO,因为氧化钙溶于水中会放出大量的热,如果温度没有变化则说明没有氧化钙,再加入盐酸,有气泡说明一定含有碳酸钙,可能含有草酸钙。草酸钙中碳元素的质量=6.4克×24/128=1.2克,而加热前草酸钙的质量为6.4g,加热一段时间后剩余固体的质量为4.8g,减少的质量为=6.4克-4.8克=1.2克,而草酸钙受热会变为一氧化碳,产生的氧化物中含有氧元素,会大于1.2克。所以该固体中含有的物质为CaCO3;CaO,即碳元素没有完全被转化。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2,MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题: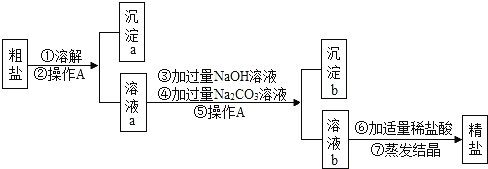
(1)实验操作A的名称是 ,该操作的目的是 .
(2)写出步骤③中发生反应的主要化学方程式 ;步骤⑥的作用是 .
(3)小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由: .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量氯化钠。为测定样品中碳酸钠的质量分数,现称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g。
计算:
(1)纯碱样品中碳酸钠的质量分数。
(2)反应后所得溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在“宏观﹣微观﹣符号”之间建立联系,是学习化学的一种重要思维方式.如图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题.
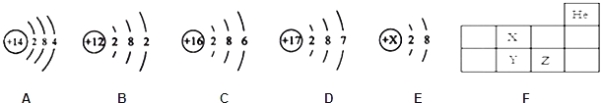
①如图A、B、C、D元素中,属于金属元素的是___________________(填元素符号);
②由B元素和D元素组成的化合物的化学式为___________________
③E粒子带2个单位负电荷,则X=___________________,离子的符号为___________________
④F为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是___________________
A.原子序数Z >Y B.核外电子数:X=Y C.Y和Z处于同一族
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你根据所学知识并结合下图所示装置回答有关问题:

(1)指出标号仪器的名称:①___________ ②______________________
(2)用高锰酸钾制取氧气的化学方程式为____________________________________________,
应选择的发生装置是___________,可以用E装置收集氧气的原因是______________________
(3)制取并收集一定量的二氧化碳,应选择的装置是______________________,欲制得干燥的二氧化碳,还需将气体通过盛有______________________(填药品名称)的洗气瓶F。
(4)用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量
水的原因是______________________,H中喷有紫色石蕊溶液的纸花显______________________色
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面的表格中列出了氯化铵在不同温度下的溶解度:
温度/℃[ | 0 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 29.4 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
(1)从表中可得到的一条信息是______ ___;
(2)20℃时,向50g水中加入20g氯化铵,形成氯化铵的__________(填“饱和”或“不饱和”)溶液,将其温度升高至60℃时,所得溶液的质量为__________;
(3)将(2)中所得的60℃时的氯化铵溶液放入如图所示的小烧杯中,在大烧杯的水中加入下列物质,能够使小烧杯中有固体析出的是__________(填字母序号);
A.冰 B.氯化钠 C.硝酸铵 D.氧化钙
(4)某同学欲配制20℃时20%的氯化铵溶液500g,需要氯化铵的质量__________.他在量取水时俯视读数,在其他操作都无误的情况下,他配制的溶液的溶质质量分数将__________(填“偏大”或“偏小”).

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com