


 步步高达标卷系列答案
步步高达标卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 时间/s | 2 | 4 | 6 | 8 | 10 |
| 质量/g | 4 | 8 | 12 | 16 | 16 |
查看答案和解析>>
科目:初中化学 来源: 题型:
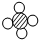 +
+
| 光照 |
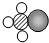 +
+
| A、图中的反应物都是单质 |
| B、该反应属于化合反应 |
| C、图中共有4种物质 |
| D、该反应不符合质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、红磷燃烧产生大量的白烟 |
| B、硫磺在空气中燃烧发出淡蓝色的火焰 |
| C、铁丝在氧气中燃烧生成红色的固体 |
| D、木炭在氧气中燃烧发出白光 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com