
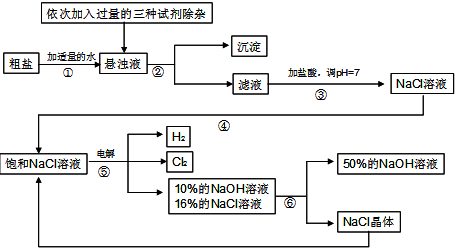
分析 (1)根据氢氧化钠的性质和用途分析判断.
(2)根据经过操作②后分出了溶液和固体,氯化钠溶液经过操作④得到了氯化钠的饱和溶液进行分析;
(3)根据氢氧化钠会与氯化镁反应,氯化钡会与硫酸钠反应,碳酸钠会与氯化钙、氯化钡反应,所以碳酸钠必须放在氯化钡之后,氢氧化钡也会与硫酸钠反应进行分析;
(4)根据饱和氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气进行分析;
(5)根据该反应的流程图进行分析.
解答 解:(1)A.氢氧化钠能去除油污,可做厨房清洁剂,说法正确;
B.氢氧化钠易溶于水,溶解时放出大量的热,说法正确;
C.氢氧化钠水溶液能使石蕊溶液变蓝,说法错误;
D.氢氧化钠具有吸水性,可用作某些气体的干燥剂,说法正确;
(2)经过操作②后分出了溶液和固体,所以操作②的名称是过滤,氯化钠溶液经过操作④得到了氯化钠的饱和溶液,所以操作④的名称是蒸发;
(3)氢氧化钠会与氯化镁反应,氯化钡会与硫酸钠反应,碳酸钠会与氯化钙、氯化钡反应,所以碳酸钠必须放在氯化钡之后,氢氧化钡也会与硫酸钠反应,所以加入顺序是③①②,Ba(OH)2溶液代替BaCl2溶液可达到同样的目的;
(4)饱和氯化钠溶液在通电的条件下生成氢氧化钠、氢气和氯气,化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(5)根据装置图可以看出,电解反应后的溶液中依然存在氯化钠,氯化钠蒸发变成饱和状态时又可以电解,所以该流程中可以循环利用的物质是氯化钠.
故答为:(1)C;(2)过滤,蒸发;(3)后.Ba(OH)2;(4)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;(5)NaCl.
点评 本题主要考查了粗盐提纯时的物质的除杂和净化,在除杂质时不要引入新的杂质,了解混合物的分离和除杂的方法.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
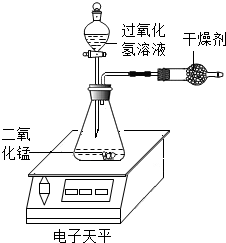 某化学兴趣小组对过氧化氢分解生成水和氧气的条件进行探究,请你参与.
某化学兴趣小组对过氧化氢分解生成水和氧气的条件进行探究,请你参与.| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| H2O2溶液浓度 | 5% | 5% | 5% | 10% | 10% | 30% | 30% |
| MnO2粉末(g) | 1.0 | 0.8 | 0.6 | 0.6 | 0.4 | 0.4 | 0.2 |
| 所用的时间(s) | 205 | 205 | 220 | 80 | 90 | 3 | 4 |
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 | 120 | 140 | 160 | 180 | 200 |
| 示数(g) | 565.40 | 565.37 | 565.34 | 565.30 | 565.28 | 565.26 | 565.24 | 565.23 | 565.22 | 565.21 | 565.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
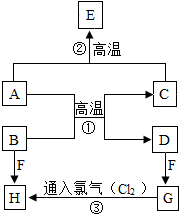 A〜H 初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G-H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:
A〜H 初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G-H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com