
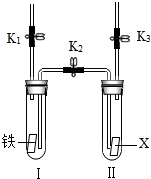
 某校小组同学利用下图装置完成了有关铁和金属X的兴趣实验.实验前检查装置气密性良好,K1、K2、K3均已关闭.
某校小组同学利用下图装置完成了有关铁和金属X的兴趣实验.实验前检查装置气密性良好,K1、K2、K3均已关闭.分析 (1)根据铁和稀硫酸反应生成硫酸亚铁和氢气进行分析;
(2)根据题中各个开关的作用进行分析;
(3)根据金属活动性顺序进行分析.
解答 解:(1)铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4═FeSO4+H2↑;
(2)通过分析可知,打开K2、K3,关闭K1,一段时间后,Ⅰ中的液体转移到Ⅱ中,其原因是:铁和稀硫酸反应生成氢气,使装置I内压强增大;
(3)A、若金属X表面无明显现象,说明X在氢之后,不一定是铜,故A错误;
B、若金属X表面有无色气泡产生,说明X是氢前金属,故B正确;
C、若金属X表面有无色气泡产生,且表面逐渐变黑,说明X的金属活动性比铁强,故C正确.
故选:BC.
故答案为:(1)Fe+H2SO4═FeSO4+H2↑;
(2)K2、K3,K1;铁和稀硫酸反应生成氢气,使装置I内压强增大;
(3)BC.
点评 本题主要考查了金属活动性顺序的应用,难度不大,注意在平时多加训练即可.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 用简炼的语言回答下列问题
用简炼的语言回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com