
| A. | AgS | B. | Ag2S | C. | Ag2O2 | D. | Ag2O |
 考前必练系列答案
考前必练系列答案科目:初中化学 来源: 题型:选择题
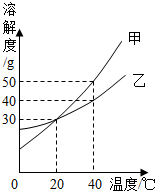 甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )| A. | 20℃时,甲溶液中溶质的质量分数一定大于乙溶液 | |
| B. | 将40℃时甲的饱和溶液降温至20℃,溶液质量不变 | |
| C. | 40℃时,分别在100g水中加入50g甲、乙,所得溶液溶质的质量分数相等 | |
| D. | 40℃时,分别在100g水中加入30g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
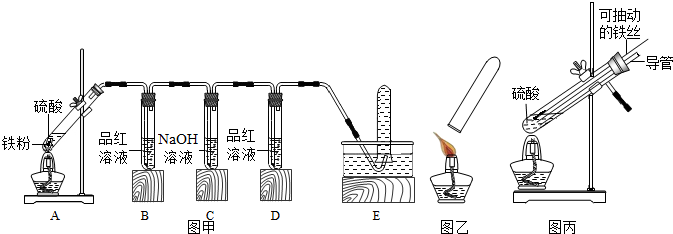
| 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有SO2和H2 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
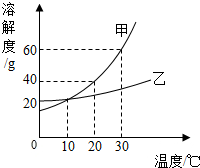 如图是甲、乙两种固体物质的溶解度曲线.据图回答:
如图是甲、乙两种固体物质的溶解度曲线.据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
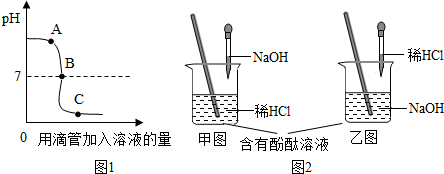
| A. | 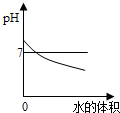 向pH=3的稀盐酸中不断加水 向pH=3的稀盐酸中不断加水 | |
| B. | 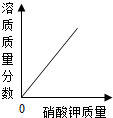 向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| C. | 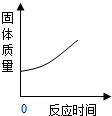 高温煅烧一定质量的石灰石 高温煅烧一定质量的石灰石 | |
| D. | 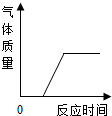 在部分变质的NaOH溶液中加稀盐酸 在部分变质的NaOH溶液中加稀盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 中和试剂 | 氢氧化钠 | 氢氧化钙 |
| 价格/(元•吨-1) | 800 | 450 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com