
)某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
|
实验次数 |
1 |
2 |
3 |
4 |
5 |
|
稀盐酸的累计加入量 |
5.0g |
10.0g |
15.0g |
20.0g |
25.0 g |
|
剩余固体的质量 |
1.5g |
1.0g |
0.5g |
0.3g |
0.3g |
请计算:
(1)2.0g石灰石样品中碳酸钙的质量为 ,石灰石中碳酸钙的质量分数为 。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。
:(1)1.7g 85% .......................(2分)
(2)设反应生成CaCl2的质量为x,CO2的质量为y 。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
1.7g x y .......................(1分)
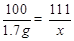
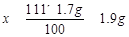 ..............................(1分)
..............................(1分)
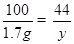
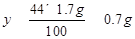 ..................................(1分)
..................................(1分)
反应后溶液的质量:1.7g+25g -0.7g =26g...............................(1分)
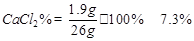 ................................(1分)
................................(1分)
[若反应后溶液质量计算为:1.7g+25g=26.7g,扣这一步的1分;CaCl2%=(1.9g÷26.7g)×100%
≈7.1%,这一步同样给1分。其它类似错误同样方法处理]
答:(1)石灰石样品中碳酸钙的质量分数为85%;(2)反应生成溶液中氯化钙的质量分数为7.3% 。
【解析】略


科目:初中化学 来源: 题型:阅读理解
 水是生命之源,人类的日常生活与工农业生产都离不开水.
水是生命之源,人类的日常生活与工农业生产都离不开水.| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | 实验步骤 | 装置图 | 实验现象 | 解释或结论 |
(1) |
在盛有20℃水的烧杯中放入一小块白磷,并通入空气 |  |
无明显变化 |
温度没有达到白磷的着火点 温度没有达到白磷的着火点 |
(2) |
在盛有50℃水的烧杯中放入一小块白磷 |  |
无明显变化 无明显变化 |
白磷没有跟空气(或氧气)接触 |
(3) |
在盛有50℃水的烧杯中放入一小块白磷,并通入空气 |  |
白磷燃烧 |
白磷与空气接触且温度达到着火点 白磷与空气接触且温度达到着火点 |
(4) |
用坩埚钳夹取一小块大理石放在酒精灯火焰上加热 |  |
无明显变化 无明显变化 |
大理石不是可燃物 |
(5) |
在燃着的蜡烛火焰上方罩一个烧杯 |  |
蜡烛熄灭 | 蜡烛与空气隔绝 蜡烛与空气隔绝 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com