

| ||
| ||
| ||
| 160 |
| x |
| 132 |
| 66g |
| 112 |
| y |
| 132 |
| 66g |


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:初中化学 来源: 题型:
| A、钢、冰水混合物、胆矾 |
| B、铜、空气、浓硫酸 |
| C、生石灰、熟石灰、食盐 |
| D、氧气、铁锈、浓盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (1)现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请计算两种氮肥的相对分子质量.
(1)现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请计算两种氮肥的相对分子质量.查看答案和解析>>
科目:初中化学 来源: 题型:
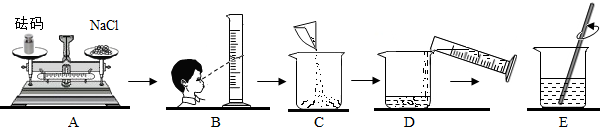
查看答案和解析>>
科目:初中化学 来源: 题型:
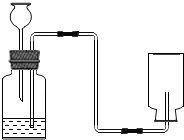 如图是实验室制取CO2装置图.
如图是实验室制取CO2装置图.查看答案和解析>>
科目:初中化学 来源: 题型:
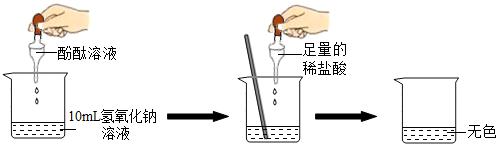
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量AgNO3的溶液 | 出现白色沉淀 | 稀HCl过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀HCl过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
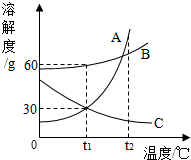 如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.请回答下列问题:
如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com