

分析 (1)变质的氢氧化钠常会含有碳酸钠,碳酸钠与氢氧化钙反应会生成碳酸钙与氢氧化钠,过量的氢氧化钙会把碳酸钠清除的更干净一些.
(2)滤液B中会含有剩余的氢氧化钙及氢氧化钠两种溶质,由氢氧化钠和氢氧化钙的溶解度与温度的关系可确定分离它们的方式;
【解决问题】根据样品与石灰水反应生成沉淀碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
【交流与反思】根据因为样品中有水,无法测出样品的氢氧化钠的质量解答.
解答 解:
(1)变质的氢氧化钠常会因氢氧化钠与二氧化碳反应含有碳酸钠,碳酸钠与氢氧化钙反应会生成碳酸钙与氢氧化钠,为把碳酸钠清除的更干净一些常会加入过量的氢氧化钙.
故答案为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;将溶液中的碳酸钠完全转化为氢氧化钠.
(2)由于溶液中加入了过量的氢氧化钙,所以滤液中会含有氢氧化钠与氢氧化钙,因为这两种物质的溶解度随温度的变化差异很大,故可采用降温结晶的方式进行分离.
故答案为:Ca(OH)2;NaOH;降温结晶;
【解决问题】
设样品中碳酸钠的质量为x,
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100
x 10g
$\frac{106}{x}=\frac{100}{10g}$
解得x=10.6g
所以:$\frac{10.6g}{16.4g}$×100%=64.6%,所以答案为:64.6%.
并把生成的气体通入澄清的石灰水中,石灰水变浑浊.
【交流与反思】
因为样品中有水,无法测出样品的氢氧化钠的质量,所以以上数据不能计算出样品中氢氧化钠的质量分数,所以答案为:样品中有水,无法测出样品的氢氧化钠的质量.
答案:
(1)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;将溶液中的碳酸钠完全转化为氢氧化钠;
(2)Ca(OH)2;NaOH;
【解决问题】64.6%.
【交流与反思】样品中有水,无法测出样品的氢氧化钠的质量.
点评 此题是对溶解度知识及混合物分离的有关知识考查,解题的关键是结合利用溶解度知识对混合物的分离进行探讨,属常规性混合物分离的题目.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:选择题
| A. |  闻气体气味 | B. |  取用块状固体 | C. | 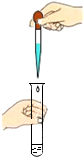 滴加液体 | D. |  稀释浓硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )| A. | 属于金属元素 | B. | 相对原子质量为238.0g | ||
| C. | 原子的核电荷数是92 | D. | 该元素的核外电子数为92 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +4 | B. | +5 | C. | +6 | D. | +7 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题

| A. | 在t1℃时,溶解度甲=乙<丙 | |
| B. | 从乙饱和溶液中析出较多量的晶体通常可采用降温结晶法 | |
| C. | 等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙 | |
| D. | t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液的溶质质量分数增大,丙溶液的溶质质量分数减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com