
【题目】下列四个图像中,不能正确表示对应变化关系的是 ( )
|
|
|
|
A.向一定量稀硫酸中加水稀释 | B.一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | C.加热一定质量的 高锰酸钾固体 | D.向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液 |
A. A B. B C. C D. D
【答案】D
【解析】A、向一定量稀硫酸中加水稀释,酸性减弱,pH值增大,无限接近于7,故A正确;B、一定温度下,向不饱和硝酸钾溶液中加入硝酸钾,一定温度下,一种固体物质的溶解度是固定的,不饱和硝酸钾溶液中随着硝酸钾的加入,溶质质量不断增加,直至饱和,所以随着硝酸钾的加入,溶液质量不断增加,饱和时达一定值,故B正确;C、加热一定质量的高锰酸钾固体,生成锰酸钾和氧气,反应后固体中锰元素质量分数先增加后达一定值,故C错误;D、向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液,氢氧化钠先与稀硫酸反应生成硫酸钠和水,再与硫酸铜溶液反应生成硫酸钠和氢氧化铜蓝色沉淀,故D正确。
点睛∶向硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液,氢氧化钠先与稀硫酸反应生成硫酸钠和水,再与硫酸铜溶液反应生成硫酸钠和氢氧化铜蓝色沉淀。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映其对应操作的是
A | B | C | D |
|
|
|
|
在一定量的AgNO3溶液中逐滴加入NaCl溶液 | 等质量Zn和Mg分别与足量的等浓度稀硫酸反应 | 向NaOH溶液中逐滴加入稀盐酸 | 等质量CaCO3分别与足量的等浓度稀盐酸反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某粗盐样品中含有杂质氯化镁、氯化钙。康康设计了以下提纯方案:
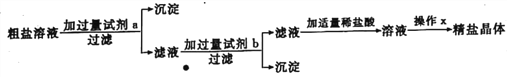
(1)过滤和操作x中都用到的玻璃仪器是____________,其在操作x中的作用是__________。
(2)加入试剂b后,必须过滤,否则滴加稀盐酸后沉淀会溶解,沉淀溶解的化学方程式为_________________。(只写1个)。
(3)滴加稀盐酸时产生气体的情况如图所示,OA段发生反应的化学方程式为_____________________。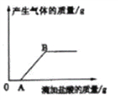
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图中提供的信息,请回答下列问题:
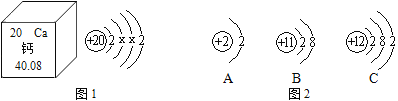
(1)由图1可知,钙的相对原子质量为________________,x=______________。
(2)图2中与钙元素化学性质相似的是________________;
(3)ABC中位于同周期的是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图的实验常用仪器回答有关问题。
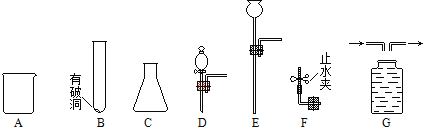
(1)仪器A的名称______________。
(2)若用过氧化氢制备氧气并控制反应速率,应选用上述仪器中的_____(填序号),其化学反应方程式为______。
(3)若用Zn和稀硫酸制备氢气并使反应随时发生或停止,应选仪器_____(填序号),其反应方程式为____。
①用充满水的G收集H2,请将图G补画完整。
②为了获得纯净的硫酸锌晶体,可先加入过量的________或________除去制H2后溶液中过量的酸,过滤,______,降温结晶,得到硫酸锌晶体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的该固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的质量与所滴入稀盐酸的质量关系曲线如下图所示:求
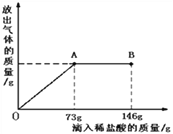
⑴恰好反应时,消耗盐酸中的溶质质量。
⑵此时,所得溶液(所得溶液为不饱和溶液)中溶质的质量分数(计算结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并按要求填空。
(1)工业上用一氧化碳和赤铁矿(主要成分是三氧化二铁)在高温下炼铁:__________。
(2)生石灰作为干燥剂: ____________________,该反应属于_________ (选填“放或吸热”)。
(3)用氢氧化钠溶液吸收少量二氧化硫气体:___________________________________。
(4)用稀硫酸除去铁锈:_____________________,反应后所得溶液的颜色为_________色。
(5)硫酸铵固体和氢氧化钙固体混合研磨:___________,该反应的基本反应类型是_______。
(6)生成沉淀的中和反应:_________________________________,恰好完全反应后液体的导电性比反应前的______ (选填“增强”、“减弱”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的甲、乙两同学围绕Na2CO3进行了如图一所示的实验.实验结束后,丙同学把A、B两支试管中的物质倒入同一洁净的烧杯中(如图二),充分混合后发现白色沉淀明显增加,结合题目信息,回答以下问题:
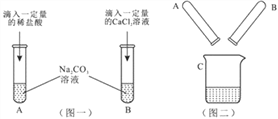
(1)甲同学的实验完成后,A试管一定有剩余的物质是_________。
(2)B试管的实验发生的化学方程式是________________。
小组同学将C中液体过滤后,对所得滤液的主要成分进行了如下探究:
【猜想与假设】实验小组的同学对滤液的成分作出了如下猜想:
猜想一:滤液中的溶质是NaCl、Na2CO3
猜想二:滤液中的溶质是_______。。
猜想三:滤液中的溶质是NaCl、CaCl2、Na2CO3
猜想四:滤液中的溶质是NaCl
【讨论与交流】通过认真讨论,小组同学排除了其中一种不合理的猜想。
(3)你认为不合理的猜想是_______,理由是______。
【进行实验】丁同学取少量滤液置于试管中,向试管中滴加一种物质,发现有无色气泡生成。
(4)你认为丁同学向滤液中滴加的物质是_________。
【实验结论】通过探究,小组同学得出了猜想一成立的结论。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钢铁行业是我国国民经济的支柱性产业,我国钢铁生产总量占世界钢铁生产总量的50%以上。
⑴钢是一种铁合金,其硬度比纯铁________(填“大”或“小”),钢铁生锈实际是铁与空气中的________发生了化学反应。请写出一种能防止钢铁生锈的措施______________。
⑵下图是某兴趣小组用实验室装置模拟炼铁的化学原理图,用于测定赤铁矿中氧化铁的质量分数。
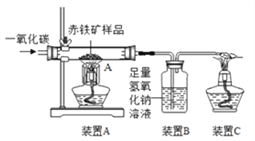
①装置A中发生反应的化学方程式为___________;装置B中发生反应的化学方程式为________;装置C的作用是______________;
②装置气密性良好,假设反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg,则要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是____________或_____________。
⑶某研究性学习小组将Fe和Fe2O3的混合物与稀硫酸反应以测定混合物中Fe2O3的质量分数。称取样品27.2g,与质量分数为20%的稀硫酸充分反应,当加入196g稀硫酸时固体粉末恰好完全溶解,此时收集到0.2g氢气,请写出Fe和Fe2O3分别与稀硫酸反应的化学方程式__________、_________。
【提出疑问】小明根据已有知识推断固体溶解后溶液中的溶质为Fe2(SO4)3和________,并据此计算出铁的质量5.6g,进一步计算发现需要硫酸的总质量比实际消耗的________(填“多”或“少”)。
【查阅资料】Ⅰ、含Fe3+的溶液中滴加硫氰化钾(KSCN)溶液后溶液呈红色;含Fe2+的溶液中滴加硫氰化钾溶液后溶液无明显现象。
Ⅱ、Fe2(SO4)3+Fe= 3FeSO4
【继续探究】小明向反应后的溶液中滴加KSCN溶液,无明显现象。则溶液中肯定不含________。
【分析计算】计算出27.2gFe和Fe2O3的混合物中Fe2O3的质量分数______。(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com