
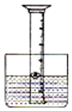
 某化学兴趣小组,设计了如右图所示装置来研究空气中氧气的体积分数:用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升.向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.
某化学兴趣小组,设计了如右图所示装置来研究空气中氧气的体积分数:用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升.向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.分析 (1)浓硫酸溶于水放热,为反应提供热量;
(2)根据金属铜具有良好的导热性,并且化学性质稳定来回答此题;
(3)从实验的目的出发来回答就容易了,此实验目的是研究空气中所含氧气的体积;
(4)量筒是用来测量液体的体积的,不能用作反应容器.
解答 解:(1)浓硫酸溶于水时发出大量的热,使得温度升高,温度达到白磷的着火点以上,白磷就会燃烧,从而达到实验的目的,故答案为:浓硫酸溶于水放热,使温度达到白磷的着火点以上;
(2)金属铜具有良好的导热性,并且化学性质稳定,不会影响实验的准确性,故答案为:铜导热性好且化学性质稳定;
(3)此实验是为了研究空气中所含氧气的体积,根据教材所学氧气约占空气总体积的五分之一这一结论,可以计算40mL-40mL×$\frac{1}{5}$=32mL; 故答案为:32mL;
(4)根据教材所学我们知道,量筒是用来测量液体的体积的,不能用作反应容器,故答案为:量筒不能用作反应容器.
故答案为:
(1)浓硫酸溶于水放热,使温度达到白磷的着火点以上;
(2)铜导热性好且化学性质稳定;
(3)32;
(4)量筒不能用作反应容器.
点评 此题是一道综合实验题,所考查的知识点较多,而且十分细致,需要同学们对实验十分熟悉才可以准确回答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克•厘米-3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属活动性顺序:Fe>X>Ag | |
| B. | 滤渣中一定含有Fe | |
| C. | 滤液中一定含有X的阳离子和Fe2+ | |
| D. | 向滤液中滴加稀盐酸,一定产生白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H+、Cl-、HCO${\;}_{3}^{-}$ | B. | Na+、Ca2+、OH- | ||
| C. | Ba2+、Cl-、CO${\;}_{3}^{2-}$ | D. | H+、Mg2+、SO${\;}_{4}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com