






科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
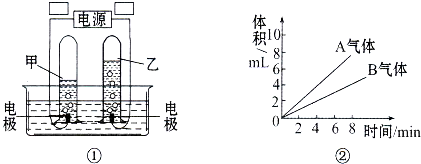
 如图是电解水的简易装置:
如图是电解水的简易装置:查看答案和解析>>
科目:初中化学 来源: 题型:
 小明同学参加学校的化学实验技能竞赛,他抽到的试题内容如下:有一包白色固体可能含有BaCl2、KNO3、CuSO4、Na2CO3中的一种或几种,请设计合理的实验方案,通过实验得出有关结论.经过一番思考,小明决定通过如下步骤进行实验,以得出相关结论.
小明同学参加学校的化学实验技能竞赛,他抽到的试题内容如下:有一包白色固体可能含有BaCl2、KNO3、CuSO4、Na2CO3中的一种或几种,请设计合理的实验方案,通过实验得出有关结论.经过一番思考,小明决定通过如下步骤进行实验,以得出相关结论.查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com