
【题目】元素周期律的发现,使化学学习和研究变得有规律可循,下表列出的是1-18号元素的部分最高正化合价和最低负化合价,阅读并回答下列问题:
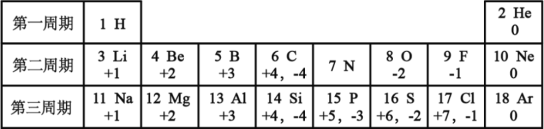
(1)12号元素属于_____(填“金属”或“非金属”)元素,它在化学反应中形成的离子与_____(填元素名称)原子具有相同的核外电子排布。
(2)氮元素的原子核外电子数为_____,其最低负化合价与氢形成的化合物的化学式为_____,该物质溶于水后形成的溶液显_____(填“酸性”、“碱性”或“中性”);某化合物中同时含有氮元素的最高正化合价和最低负化合价,写出该化合物的化学式并标出氮元素的化合价_____。
(3)第三周期元素化合价变化的趋势是_____。
(4)碳元素形成的物质种类很多,其中C和CO是初中化学常见的还原剂,当它们作还原剂时,碳元素的化合价均_____(填“上升”、“下降”或“不变”)。请判断反应NaH+H2O=NaOH+H2↑中,作还原剂的是_____(填化学式)。
【答案】金属 氖 7 NH3 碱性 ![]() 除氩元素外,从左到右,元素最高正化合价由+1 价到+7 价依次增加,且数值等于元素原子的最外层电子数。从硅到氯,最低负化合价由-4 价到-1 价依次递增。金属无负价, 稀有气体只有 0 价 上升 NaH
除氩元素外,从左到右,元素最高正化合价由+1 价到+7 价依次增加,且数值等于元素原子的最外层电子数。从硅到氯,最低负化合价由-4 价到-1 价依次递增。金属无负价, 稀有气体只有 0 价 上升 NaH
【解析】
(1)12号元素是镁元素,属于金属元素,失去电子后,形成的镁离子与氖原子具有相同的核外电子排布;
(2)氮原子核外有7个电子,最外层有5个电子,最低价为-3价,最高价为+5,氢元素显+1价,其最低负化合价与氢形成的化合物的化学式为NH3,氨气溶于水形成氨水,显碱性;硝酸铵中含有氮元素的最高正化合价和最低负化合价,在铵根中氮元素显-3价,在硝酸根中显+5价,可表示为:![]() ;
;
(3)第三周期,从左到右,元素最高正化合价由+1价到+7价依次增加,且数值等于元素原子的最外层电子数;从硅到氯,最低负化合价由-4价到-1价依次递增;金属无负价,稀有气体只有0价;
(4)C和CO是初中化学常见的还原剂,当它们作还原剂时,化合价均升高;由题目的提示可得,所含元素化合价在反应后升高的反应物为还原剂,同时按照题目给出的钠元素化合价仅+1价,以及NaH化学式的写法,可以推出该物质中氢元素化合价为-1价,在反应后升高至氢气中氢元素的化合价为0价,因而NaH为还原剂。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:初中化学 来源: 题型:
【题目】下表是 KNO3 在不同温度下的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度(g/100g 水) | 13.3 | 31.6 | 63.9 | x | 169 | 246 |
①表中“63.9”的含义是 ___。
②20℃将 31gKNO3 固体放入 50g 水中,所得溶液的质量是 ___g,若升温到 40℃所得溶液的溶质质量分数是 ___(精确到 0.1%)。
③从硝酸钾溶液中获取晶体的最佳方法是 ___。
④为测定 x 的值,取 4 份 60℃的水各 50g,分别进行实验,并记录数据如下表:
实验编号 | 甲 | 乙 | 丙 | 丁 |
KNO3 的质量/g | 40 | 50 | 60 | 70 |
H2O 质量/g | 50 | 50 | 50 | 50 |
溶液质量/g | 90 | 100 | 105 | 105 |
由实验可知 ___。
A 甲所得溶液中溶质质量分数为 80%
B 乙和丙所得溶液溶质质量分数相等
C 丙和丁所得溶液中含溶质质量相等
D 60℃时 KNO3 的溶解度为 110g/100g 水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2014年5月7日在南京丢失的放射源铱﹣192,于5月10日安全回收.铱﹣192常用于肿瘤治疗.下图是铱﹣192在元素周期表中的信息,有关铱的说法不正确的是
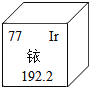
A. 铱的元素符号是Ir B. 铱元素是非金属元素
C. 铱原子的原子序数为77 D. 铱元素的相对原子量为192.2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下图是利用海水提取粗盐的过程:
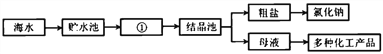
上图中①是_____池 (填“蒸发”或“冷却”)。
(2)粗盐中含有少量 CaCl2、MgCl2、Na2SO4 和泥沙,某同学将该粗盐样品进行提纯。
①将样品加适量水溶解,然后进行_____,除去泥沙等难溶性杂质,得到澄清溶液;
②向所得的澄清溶液中依次加入稍过量的 BaCl2 溶液、NaOH 溶液和_____溶液, 除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯挣的 NaCl 溶液;
③蒸发溶液,得到较多氯化钠固体时停止加热,他注意到不能立即把_____直接放 在实验台上,以免烫坏实验台。
(3)另一同学用所得的氯化钠和蒸馏水配制溶质质量分数为 6%的氯化钠溶液。配制步骤:①称量和量取②溶解③计算④装入试剂瓶贴好标签。配制上述溶液的正确顺序是_______ (填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁合金广泛用于航空航天、导弹、汽车、建筑等行业。镁元素的相关信息如图所示。请回答下列问题:
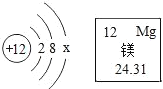
(1)镁原子的质子数为_____,x值为_____。
(2)镁属于元素_____(填“金属”或“非金属”),金属镁在化学反应在容易_____(填写“得到”或“失去”)电子。
(3)海水中含有丰富的氯化镁,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如图:
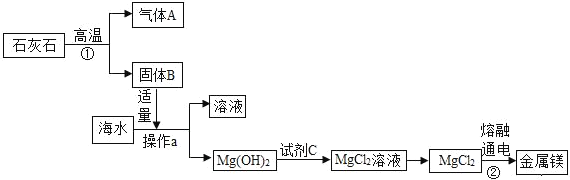
在上述流程中,通过操作a分离出固体Mg(OH)2,操作a的名称是_____,试剂C为:_____。
反应①的化学方程式为_____。
反应②的化学方程式为_____。
(4)上述流程中没有涉及到的基本反应类型是_____反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取某些气体的装置如图,回答有关问题。

(1)若选用装置A和F组合制取氧气,其化学方程式可以为_____,选用F装置收集氧气的原因是_____。
(2)若选用装置B作为制取二氧化碳的发生装置,其中试管的作用是_____。(填1种即可)
(3)若选用装置C作为制取氢气的发生装置,添加稀硫酸时,液面最好添加到如图_____处(填字母“a”、“b”或“c”)。
(4)实验室用73g质量分数为10%的盐酸与足量大理石反应,最多能生成二氧化碳的质量是多少?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上生产电路板及处理废液的工艺流程图如下:
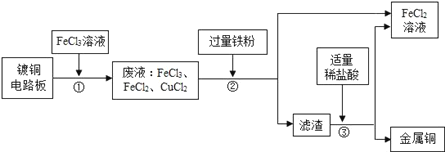
(1)FeCl3与铜反应生成的产物是___和___。
(2)步骤②中加入的铁粉能与废液中的FeCl3发生化合反应,完成化学方程式:Fe+2FeCl3═3___;同时还发生反应的化学方程式为___,该反应属于___。(填写基本反应类型)
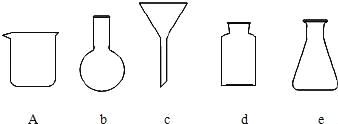
(3)步骤②需要进行___操作,为完成该操作需要下图中的___ (填字母序号),同时还需用到的玻璃仪器是___,其作用是___。
(4)步骤②③所得的FeCl2可与一种单质发生化合反应生成FeCl3,从而实现物质的循环利用,则该单质的化学式为___。
(5)若步骤②后的滤渣为80g,步骤③中用掉了稀盐酸250g,最后得到金属铜66g,通过计算了解所使用的稀盐酸的溶质质量分数是___?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图,海水淡化可采用膜分离技术,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各离子不能通过淡化膜,从而得到淡水.对加压后右侧海水成分变化进行分析,正确的是( )
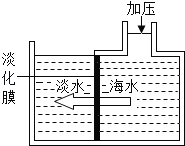
A.溶质质量增加 B.溶剂质量减少
C.溶液质量不变 D.溶质质量分数减少
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲同学用如图所示装置制得CO2,并验证CO2能与水反应生成酸的性质。
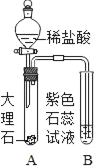
B试管发生的现象是_____,反应方程式是_____。
乙同学在实验时闻到制得的CO2有些刺激性气味,于是乙同学对气味的来源以及能使紫色石蕊溶液变红的酸性物质进行如下探究:
(查阅资料)大理石与稀盐酸反应产生热量;大理石无气味,稀盐酸有刺激性气味。
(提出猜想)刺激性气味来源于稀盐酸,并且混入与:
I.温度有关 II._____ III.温度及气流的速率有关
(进行实验)实验装置如下(三个实验中所用稀盐酸及紫色石蕊溶液的体积、溶质的质量分数均相同;夹持装置已略去)。
编号 | 实验装置及操作 | 实验现象与结论 |
1 |
| 一段时间内无现象。 |
2 |
| 紫色石蕊试液变红,_____成立。 |
3 |
| _____,猜想II成立。综上猜想III成立。 |
(拓展与思考)
(1)需在装置A、B之间增加装置C.装置C的作用是_____,装置C中药品应具有的性质是_____。
(2)将实验1的稀盐酸改为浓盐酸,紫色石蕊试液变红,说明浓盐酸具有的物理性质是_____。
(3)有同学认为实验1可以省去不做也可以验证猜想。你的观点是_____(填“能”或“不能”)验证猜想。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com