
”¾ĢāÄæ”æĻĀĮŠŹµŃéÉč¼ĘÄÜ»ńµĆ³É¹¦µÄŹĒ£Ø””””£©
A. 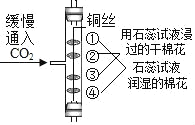 Ö¤Ć÷CO2ĆܶȱČæÕĘų“óĒŅÄÜÓėĖ®·“Ó¦²śÉśĖį
Ö¤Ć÷CO2ĆܶȱČæÕĘų“óĒŅÄÜÓėĖ®·“Ó¦²śÉśĖį
B. 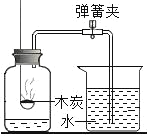 ²ā¶ØæÕĘųÖŠŃõĘųµÄŗ¬Įæ
²ā¶ØæÕĘųÖŠŃõĘųµÄŗ¬Įæ
C. 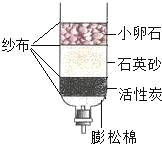 ½«ŗÓĖ®×Ŗ»ÆĪŖ“æ¾»Ė®
½«ŗÓĖ®×Ŗ»ÆĪŖ“æ¾»Ė®
D. 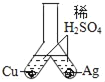 ŃéÖ¤CuŗĶAgµÄ½šŹō»ī¶ÆŠŌ“óŠ”
ŃéÖ¤CuŗĶAgµÄ½šŹō»ī¶ÆŠŌ“óŠ”
”¾“š°ø”æA
”¾½āĪö”æ
A”¢ŹµŃé¹ż³ĢÖŠ£¬¢Ś”¢¢ŪĪŽĆ÷ĻŌĻÖĻó£¬ĖµĆ÷¶žŃõ»ÆĢ¼²»ÄÜŹ¹ŹÆČļ±äÉ«£¬¢Ü”¢¢ŁĻČŗó±äŗģÉ«£¬ĖµĆ÷¶žŃõ»ÆĢ¼ĆܶȱČæÕĘų“ó£¬ÄÜŗĶĖ®·“Ӧɜ³ÉĢ¼Ėį£¬Ģ¼ĖįŹ¹ŹÆČļŹŌŅŗ±äŗģÉ«£¬·ūŗĻĢāŅā£»
B”¢Ä¾ĢæČ¼ÉÕÉś³É¶žŃõ»ÆĢ¼£¬ĻūŗÄŃõĘųµÄĶ¬Ź±Éś³É¶žŃõ»ÆĢ¼ĘųĢ壬µ¼ÖĀĖ®²»ÄܽųČė¼ÆĘųĘ棬²»Äܲā¶ØŃõĘųŗ¬Į棬²»·ūŗĻĢāŅā£»
C”¢ŹµŃé¹ż³ĢÖŠ£¬Ķعż¹żĀĖæÉŅŌ°Ń²»ČÜÓŚĖ®µÄĪļÖŹ³żČ„£¬Ķعż»īŠŌĢææÉŅŌĪüø½É«ĖŲ”¢ŅģĪ¶µČĪļÖŹ£¬µ«ŹĒŅ×ČÜÓŚĖ®µÄĪļÖŹ²»ÄܳżČ„£¬²»Äܽ«ŗÓĖ®×Ŗ»ÆĪŖ“æ¾»Ė®£¬²»·ūŗĻĢāŅā£»
D”¢ŹµŃé¹ż³ĢÖŠ£¬ĪŽĆ÷ĻŌĻÖĻó£¬ĖµĆ÷½šŹō»ī¶ÆŠŌĖ³ŠņÖŠĶŗĶŅų¶¼ÅÅŌŚĒāŗóĆę£¬µ«ŹĒ²»ÄÜÅŠ¶ĻĶŗĶŅųµÄ»īĘĆŠŌ£¬²»·ūŗĻĢāŅā”£¹ŹŃ”A”£


 ŹżŃ§°ĀČüŹī¼ŁĢģĢģĮ·ÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø
ŹżŃ§°ĀČüŹī¼ŁĢģĢģĮ·ÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅ³£ÓƶžŃõ»ÆĆĢÓėÅØŃĪĖįÖʱøĀČĘų£¬·“Ó¦ŌĄķĪŖ£ŗMnO2+4HCl(ÅØ)![]() MnCl2+Cl2”ü+2H2O£®
MnCl2+Cl2”ü+2H2O£®
ŹµŃé×°ÖĆČēĶ¼1ĖłŹ¾£®
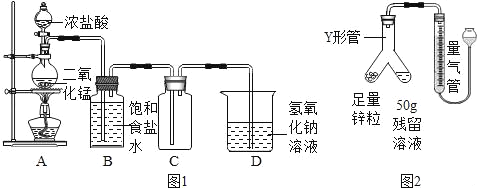
£Ø²éŌÄ׏ĮĻ£©
¢ŁĀČĘųŹĒ»ĘĀĢÉ«ĒŅÓŠ¶¾µÄĘųĢ壬ÄŃČÜÓŚ±„ŗĶŹ³ŃĪĖ®£®
¢ŚĀČĘųÄÜÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬Éś³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘ(NaClO)ŗĶĖ®£®
¢Ū³£ĪĀ³£Ń¹ĻĀ£¬ĒāĘųµÄĆܶČĪŖ0.09g/L£®
£Ø»Ų“šĪŹĢā£©
(1)×°ÖĆBµÄ×÷ÓĆĪŖ___£®
(2)øł¾Ż×°ÖĆCÅŠ¶Ļ£ŗĀČĘųµÄĆܶȱČæÕĘų___(Ģī”°“ó”±»ņ”°Š””±)
(3)×°ÖĆDµÄ×÷ÓĆĪŖ___(ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾)£®
£Ø·¢ĻÖĪŹĢā£©
Öʱø¹ż³ĢÖŠ£¬ŅņŃĪĖįÅضČĻĀ½µµ¼ÖĀ·“Ó¦Ķ£Ö¹£®Ä³»ÆѧŠ”×éĶ¬Ń§ĪŖ²ā¶Ø×°ÖĆAÖŠ·“Ó¦ŗó²ŠÓąŅŗÖŠHClµÄÖŹĮæ·ÖŹż£¬Ģį³öĮ½Ģײā¶Ø·½°øČēĶ¼3ĖłŹ¾£®
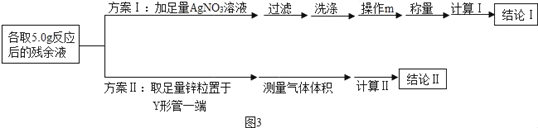
(4)·½°ø¢ńÖŠ²Ł×÷mµÄĆū³ĘĪŖ___£¬Ķعż³ĘĮæÉś³É³ĮµķµÄÖŹĮ棬¼ĘĖć³ö²ŠÓąŅŗÖŠHClµÄÖŹĮæ·ÖŹż£¬“Ė²ā¶Ø·½°øŹĒ___(Ģī”°æÉŠŠ”±»ņ”°²»æÉŠŠ”±)µÄ£¬ŌŅņŹĒ___£»
(5)·½°ø¢ņĄūÓĆĶ¼2×°ÖĆ(¹Ģ¶ØŅĒĘ÷µÄ×°ÖĆŅŃĀŌ)½ųŠŠ²ā¶Ø£®
¢ŁŹµŃé¹ż³ĢÖŠ¹Ū²ģµ½ŠæĮ£±ķĆęÓŠĘųÅŻ²śÉś£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___£»
¢Ūµ±×°ÖĆ»Öø“ÖĮ³£ĪĀŹ±£¬²āµĆ·“Ӧɜ³ÉĘųĢåµÄĢå»żĪŖ183.5mL£¬øł¾Ż»Æѧ·½³ĢŹ½¼ĘĖć£¬²ŠÓąŅŗÖŠHClµÄÖŹĮæ·ÖŹżĪŖ____£æ
£Ø·“Ė¼ĢÖĀŪ£©
(6)ĪŖĮĖ±£Ö¤·½°ø¢ņ²ā¶Ø½į¹ūµÄ×¼Č·ŠŌ£¬ÕżČ·²Ł×÷ŹĒ£ŗĒ抱YŠĪ¹Ü£¬___(Ģī±źŗÅ)
A ½«²ŠÓąČÜŅŗ×ŖŅʵ½ŠæĮ£ÖŠ B ½«ŠæĮ£×ŖŅʵ½²ŠÓąČÜŅŗÖŠ
(7)YŠĪ¹ÜÄŚæÕĘų¶ŌĘųĢåĢå»żµÄ²āĮæ___(Ģī”°ÓŠ”±»ņ”°Ć»ÓŠ”±)Ó°Ļģ£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøĘŌŖĖŲŹĒČĖĢå²»æÉ»ņȱµÄŌŖĖŲ£¬Ėü¼ČŹĒÉķĢåµÄ¹¹ŌģÕߣ¬ÓÖŹĒÉķĢåµÄµ÷½ŚÕß”£Ķ¼ĪŖij¶łĶÆøĘʬµÄÉĢĘ·±źĒ©£¬Ēėøł¾Ż±źĒ©µÄÓŠ¹ŲŠÅĻ¢Ķź³ÉĻĀĮŠø÷Ģā£ŗ

(1)“Ė¶łĶÆøĘʬŹōÓŚ___(Ģī”°“æ¾»Īļ”±”°»ģŗĻĪļ”±Ö®Ņ»)”£
(2)Ö÷ŅŖ³É·ÖĢ¼ĖįøĘ(CaCO3)ÓÉ___ÖÖŌŖĖŲ×é³É”£
(3)ŌŚĢ¼ĖįøĘ(CaCO3)ÖŠøĘŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ___¼Ū”£
(4)ĪŖ²ā¶Ø“ĖøĘʬ֊Ģ¼ĖįøʵÄŗ¬Įæ£¬Č”1.5gÕāÖÖøĘʬ£¬ĻņĘäÖŠ¼ÓČėČÜÖŹÖŹĮæ·ÖŹżĪŖ7.3%µÄĻ”ŃĪĖį£¬Éś³ÉĘųĢåµÄÖŹĮæÓėĖł¼ÓČėĻ”ŃĪĖįµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾”£
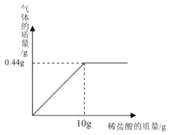
¢Ł“ĖĘųĢåĪŖ___(Š“»ÆѧŹ½)£»
¢ŚŹŌ¼ĘĖć“ĖøĘʬ֊Ģ¼ĖįøʵÄÖŹĮæ·ÖŹż_____”£(¼ĘĖć½į¹ū¾«Č·ÖĮ0.1%)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠŅ»°ü°×É«¹ĢĢåæÉÄÜŗ¬ÓŠK2SO4”¢K2CO3”¢BaCl2”¢KOHÖŠµÄŅ»ÖÖ»ņ¼øÖÖ”£Č”ÉŁĮæ°×É«¹ĢĢåČÜÓŚ×ćĮæµÄĖ®ÖŠÓŠ°×É«³Įµķ²śÉś”£¹żĀĖŗóĻņ³ĮµķÖŠµĪ¼ÓŃĪĖį£¬³ĮµķµÄĮ攢²śÉśĘųĢåµÄĮæÓė¼ÓČėŃĪĖįĢå»ż±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ÓÉ“ĖĶʶĻ°×É«¹ĢĢåÖŠ£Ø””””£©

A. æĻ¶ØÖ»“ęŌŚK2CO3
B. æĻ¶Ø²»“ęŌŚBaCl2
C. æÉÄÜ“ęŌŚK2SO4
D. °×É«¹ĢĢåæĻ¶ØÖ»ŗ¬ÉĻŹö¹ĢĢåÖŠµÄĮ½ÖÖĪļÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾ŹµŃé²Ł×÷ÕżČ·µÄŹĒ£Ø””””£©
A. 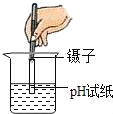 ²āČÜŅŗµÄpH B.
²āČÜŅŗµÄpH B. 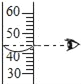 ¶Į³öŅŗĢåĢå»ż
¶Į³öŅŗĢåĢå»ż
C. 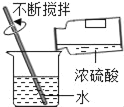 Ļ”ŹĶÅØĮņĖį D.
Ļ”ŹĶÅØĮņĖį D.  ŅĘ×ßÕō·¢Ćó
ŅĘ×ßÕō·¢Ćó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŃĄøąÖŠ,³£ÓĆĒįÖŹĢ¼ĖįøĘ·ŪÄ©×öĦ²Į¼Į”£Ķس£ŅŌŹÆ»ŅŹÆ(ŗ¬ŌÓÖŹ,¼ŁÉčŌÓÖŹ²»²ĪÓė·“Ó¦Ņ²²»ČÜÓŚĖ®)ĪŖŌĮĻ½ųŠŠÉś²ś,ĻĀĶ¼ŹĒŹµŃéŹŅÄ£ÄāÉś²ś”°Ä¦²Į¼Į”±µÄĮ÷³Ģ,Ēė»Ų“š:
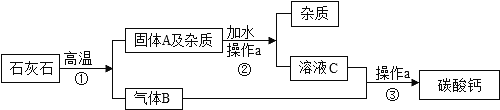
£Ø1£©ŹµŃé²Ł×÷![]() µÄĆū³ĘŹĒ________£¬½ųŠŠŹµŃé²Ł×÷
µÄĆū³ĘŹĒ________£¬½ųŠŠŹµŃé²Ł×÷![]() ÓƵ½µÄ²£Į§ŅĒĘ÷³ż²£Į§°ō”¢ÉÕ±Ķā,»¹ŠčŅŖµÄ²£Į§ŅĒĘ÷ŹĒ_________.
ÓƵ½µÄ²£Į§ŅĒĘ÷³ż²£Į§°ō”¢ÉÕ±Ķā,»¹ŠčŅŖµÄ²£Į§ŅĒĘ÷ŹĒ_________.
£Ø2£©¢Ł“¦·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________________.
£Ø3£©¹¤ŅµÉś²śÖŠ,ĪŖĮĖ½ŚŌ¼³É±¾,ÓŠŹ±»į°ŃÓŠÓƵÄÉś³ÉĪļÖŲŠĀŃ»·ĄūÓĆ,ÉĻĆęµÄ¹¤ŅÕĮ÷³ĢÖŠæÉŃ»·Ź¹ÓƵÄĪļÖŹŹĒ_________(Ģī»ÆѧŹ½).
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij“æ¼īѳʷ֊ŗ¬ÓŠÉŁĮæĀČ»ÆÄĘ£¬ĻÖČ”øĆѳʷ12gČܽāŌŚ100gĖ®ÖŠ£¬ŌŁĻņĘäÖŠÖšµĪ¼ÓČėĀČ»ÆøĘČÜŅŗ£¬²śÉśµÄ³ĮµķÓė¼ÓČėĀČ»ÆøĘČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
¼ĘĖć£ŗ
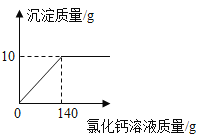
£Ø1£©“æ¼īÖŠĢ¼ĖįÄʵÄÖŹĮæ·ÖŹż![]() ½į¹ū¾«Č·µ½
½į¹ū¾«Č·µ½![]() £¬ĻĀĶ¬
£¬ĻĀĶ¬![]() ______£»
______£»
£Ø2£©Ē”ŗĆĶźČ«·“Ó¦Ź±£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼A”¢BŹĒĢ¼ŌŖĖŲŗĶµŖŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄ²æ·ÖŠÅĻ¢£¬C”¢DŹĒĮ½ÖÖĮ£×ӵĽį¹¹Ź¾ŅāĶ¼£®×ŠĻø¹Ū²ģ£¬°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
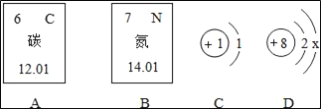
(1)Ģ¼ŌŖĖŲµÄŌ×ÓŠņŹżŹĒ___£®
(2)µŖŌŖĖŲµÄÖŹ×ÓŹżŹĒ___£®
(3)ČōDĮ£×ӵĻÆѧ·ūŗÅĪŖO2©£¬ŌņX£½___£®
(4)ÉĻŹöĖÄÖÖŌŖĖŲ¶¼ŹōÓŚ___(Ģī”°½šŹō”±»ņ”°·Ē½šŹō”±)ŌŖĖŲ£®
(5)ÉĻŹöĖÄÖÖŌŖĖŲæÉ×é³É¼øÖÖ³£¼ūµÄ»Æ·Ź£¬ĒėŠ“³öĘäÖŠŅ»ÖֵĻÆѧŹ½___£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņĖįŃĒĢśÓĆæÉÓŚÖĘ¾»Ė®¼ĮµČ£¬¹¤ŅµÉĻ³£ĄūÓĆ·ĻĢśŠ¼(ŗ¬ÉŁĮæŃõ»ÆĀĮ”¢Ńõ»ÆĢśµČ)ÖĘČ””£
(1)Č„ÓĶĪŪ£ŗÓĆČČĖ®ŗĶĻ“µÓ¼ĮČ„³ż·ĻĢśŠ¼±ķĆęµÄÓĶĪŪ£¬ĖµĆ÷Ļ“µÓ¼Į¾ßÓŠ____¹¦ÄÜ”£
(2)³żŃõ»ÆĀĮ£ŗŌŚ·ĻĢśŠ¼ÖŠ¼ÓČėČȵÄĒāŃõ»ÆÄĘČÜŅŗ£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗAl2O3+2NaOH+3R![]() 2NaAl(OH)4£¬ŌņRµÄ»ÆѧŹ½ĪŖ__”£
2NaAl(OH)4£¬ŌņRµÄ»ÆѧŹ½ĪŖ__”£
(3)ÖĘČ”ĮņĖįŃĒĢś¾§Ģ壬Į÷³ĢČēĶ¼£ŗ
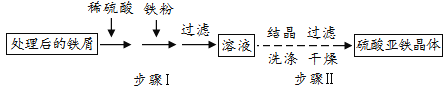
¢Ł²½Öč¢ńÖŠ£¬¼ÓČė“æ¾»Ģś·Ū£¬Ź¹ĢśÓėĮņĖįĢś·“Ӧɜ³ÉĮņĖįŃĒĢś£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ__”£
¢ŚFeSO4µÄČܽā¶ČĖęĪĀ¶Č±ä»ÆµÄĒśĻßČēĶ¼£¬²½Öč¢ńÖŠČÜŅŗ×īŗĆæŲÖĘŌŚ63”ę¹żĀĖµÄŌŅņŹĒ__”£
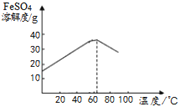
¢Ū²½Öč¢ņÖŠ¹żĀĖµĆµ½FeSO4¾§ĢåÓĆ__Ļ“µÓ(ĢīŠņŗÅ)”£
A Ė® B ĮņĖįŃĒĢśČÜŅŗ C ±„ŗĶĮņĖįŃĒĢśČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com