
| ʵ����� | 1 | 2 | 3 | 4 | 5 |
| NaOH��Һ�ۼƼ�����/g | 0.0 | 50.0 | 100.0 | 150.0 | 200.0 |
| ��ˮ��pH | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 |
���� �������ƺ�ϡ���ᷴӦ���������ƺ�ˮ��ǡ����ȫ��Ӧʱ��ҺpH=7�����ݷ�Ӧ�Ļ�ѧ����ʽ�����ṩ�����ݿ��Խ�����ط���ļ��㣮
��� �⣺��1���ɱ�����Ϣ��֪������ˮǡ�ó�����ʱ��NaOH��Һ�ۼƼ�������200.0g��
���200.0��
��2������������Ϊx��
��Ӧ��������������Ϊ��200.0g��0.4%=0.8g��
2NaOH+H2SO4�TNa2SO4+2H2O��
80 98
0.8g x
$\frac{80}{0.8g}$=$\frac{98}{x}$��
x=0.98g��
��ˮ���������������Ϊ��$\frac{0.98g}{100g}$��100%=0.98%��
���0.98%��
��3��������100.0g����������Һʱ��������Һ����Ԫ�ص������ͷ�ˮ����������Ԫ��������ȣ����������Һ����Ԫ�ص�����Ϊ��
0.98g��$\frac{32}{98}$��100%=0.32g��
���0.32��
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  �Բ���Ƭ���� | B�� |  �׳�ˮ�� | C�� |  �ֻ����� | D�� |  ��ˮɹ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�� | B�� | ԭ�� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | -3 | B�� | +3 | C�� | +4 | D�� | +5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �̬��������ʯ�һ��ʩ�ã�Ч������ | |
| B�� | ����ϴ�Ӽ�ȥ���·��ϵ����������黯���� | |
| C�� | ������������еġ��⡱Խ��Խ�� | |
| D�� | ��������������ж�����̼�ĺ������ڵ����ĺ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
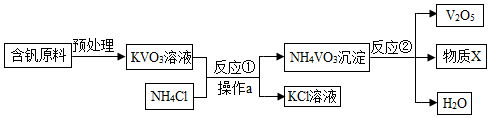
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ�ȶ��������з�Ԫ�ص���������ԼΪ50% | |
| B�� | һ�ȶ����������Է�������Ϊ86.5 | |
| C�� | һ��һ�ȶ��������������к���5��ԭ�� | |
| D�� | һ�ȶ���������̼Ԫ�ء���Ԫ�ء���Ԫ�ء���Ԫ������Ԫ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �߲�¥���Ż�ʱ�����ܳ����������� | |
| B�� | �ڼ���վ�����Ͻ��̻�ı�־ | |
| C�� | �����δ�����ĵؽѣ�Ҫ���ƻ�ʵ�� | |
| D�� | ���õ����Ż�ʱ��������ˮ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com