已知道,已知同温下,容积相等的密闭容器中,气态物质的分子数目越多.容积内的压强就越大,而且成正比例关系.根据这个知识,请完成下题:
将wg焦碳(焦碳对容积的影响忽略不计)和ng氧气同时放入一个密闭容器中,测得压强为p.提供必要条件,让容器内的物质充分反应后,恢复到原来温度,测得压强为p1,那么:
(1)如果p<p1,则w与n应满足的关系是(提示:从化学方程式反应前后气体物质的分子数是如何改变的)______.
(2)如果p=p1,则w与n应满足的关系是(提示:p=p1,说明反应前后气体分子数目有变化吗?)______.
【答案】
分析:根据在相同温度和相同体积的条件下,气体压强(P)与气体分子数目(n)成正比关系(P=kn),可判断反应前后气体的分子数目的改变;根据碳在氧气中充分燃烧与不充分燃烧的规律,此时碳应充分燃烧全部生成一氧化碳或二氧化碳,其中氧气足量或过量;根据碳在氧气中完全燃烧的化学方程式,由反应中碳与所消耗氧气的质量关系,判断密闭容器中wg碳和ng氧气的关系.
解答:解:根据题意,反应前后分子数目不变,由C+O
2
CO
2与2C+O
2
2CO,可判断碳在氧气中充分燃烧生成二氧化碳,分子数目变大则只生成一氧化碳或一氧化碳二氧化碳共存.
假设ag碳和bg氧气恰好完全反应生成二氧化碳,则
C+O
2
CO
212 32
wg ng
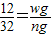
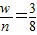
假设ag碳和bg氧气恰好完全反应生成一氧化碳,则
2C+O
2
2CO
2×12 32
wg ng
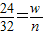
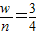
(1)如果p
<p
1,则生成的气体分子数变多,可以是只生成一氧化碳,也可是即生成二氧化碳由生成一氧化碳,则w与n应满足的关系是
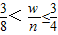
(2)如果p
=p
1,此时只发生生成二氧化碳的反应,
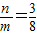
,若容器中氧气有剩余,反应前后分子数目也不变,反应前后压强也相同,因此,容器中碳的质量
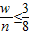
.
故答案为:(1)
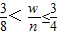
(2)
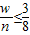
.
点评:根据碳在氧气中完全燃烧与不完全燃烧前后气体的分子个数关系,判断该题中所发生反应为完全燃烧生成二氧化碳,是解决问题的关键.

 CO2与2C+O2
CO2与2C+O2 2CO,可判断碳在氧气中充分燃烧生成二氧化碳,分子数目变大则只生成一氧化碳或一氧化碳二氧化碳共存.
2CO,可判断碳在氧气中充分燃烧生成二氧化碳,分子数目变大则只生成一氧化碳或一氧化碳二氧化碳共存. CO2
CO2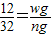
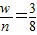
 2CO
2CO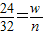
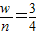
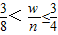
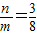 ,若容器中氧气有剩余,反应前后分子数目也不变,反应前后压强也相同,因此,容器中碳的质量
,若容器中氧气有剩余,反应前后分子数目也不变,反应前后压强也相同,因此,容器中碳的质量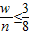 .
.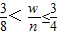
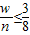 .
.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案