
分析 根据常见元素的化合价和化合物中正负化合价代数和为0的规则进行计算可求出其他元素的化合价.
解答 解:氧化铝的化学式为Al2O3,已知铝元素的化合价为+3,根据化合物中正负化合价的代数和为0的规则,可推出氧元素的化合价为-2;
氯化铁的化学式为FeCl3,已知铁元素的化合价为+3,根据化合物中正负化合价的代数和为0的规则,可推出氯元素的化合价为-1;
氯酸钾的化学式为KClO3,已知钾元素的化合价为+1,氧元素的化合价为-2,根据化合物中正负化合价的代数和为0的规则,可推出氯元素的化合价为+5;
高锰酸钾的化学式为KMnO4,已知钾元素的化合价为+1,氧元素的化合价为-2,根据化合物中正负化合价的代数和为0的规则,可推出锰元素的化合价为+7;
铜为单质,化学式为Cu,铜元素的化合价为0,
氧气为单质,化学式为O2,氧元素的化合价为0.
故答案为:$\stackrel{+3}{Al}$2$\stackrel{-2}{O}$3;$\stackrel{+3}{Fe}$$\stackrel{-1}{Cl}$3;$\stackrel{+1}{K}$$\stackrel{+5}{Cl}$$\stackrel{-2}{O}$3;$\stackrel{+1}{K}$$\stackrel{+7}{Mn}$$\stackrel{-2}{O}$4;$\stackrel{0}{Cu}$;$\stackrel{0}{O}$2.
点评 本题考查化合价规律,并要求记忆常见元素的化合价,会根据化学式确定元素的化合价.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度 溶解度 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| NaCl | 35.8 | 36 | 36.3 | 36.6 | 37.0 | 37.3 | 37 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 A~H是初中化学常见的物质,已知A、B均为黑色固体,D为紫红色固体单质,F为红棕色粉末,它们的转化关系如图所示,请回答:
A~H是初中化学常见的物质,已知A、B均为黑色固体,D为紫红色固体单质,F为红棕色粉末,它们的转化关系如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe CaO | B. | Cu CaO | C. | Fe Ca(OH)2 | D. | Cu CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 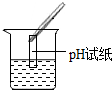 |  |  |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com