
分析 (1)利用相关的物质在空气中的变化情况解决此题.
(2)金属钠和盐溶液的反应先是和里面的水的反应生成氢氧化钠和氢气.
解答 解:(1)A、浓盐酸具有较强的挥发性,敞口放置会不断挥发出氯化氢气体导致溶液质量减少.
B、浓硫酸具有吸水性,在空气中敞口放置易吸水导致溶液质量增加.
C、氢氧化钠溶液能与二氧化碳并发生反应,导致自身质量增加.
D、生石灰与空气中的水反应生成氢氧化钙且导致质量增加.
E、酒精具有挥发性,质量减小.
F、铁粉易生锈,质量增加
因此,可按照敞口放置时质量是否增加进行分类.
故填:敞口放置时质量增加;BCDF.
(2)钠与水反应生成的氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故总的反应方程式为:2Na+2H2O+CuSO4═Cu(OH)2↓+Na2SO4+H2↑,故填:2Na+2H2O+CuSO4═Cu(OH)2↓+Na2SO4+H2↑.
点评 此题是对常见物质特性的考查,要了解常见酸碱盐的挥发性、吸水性和吸收空气中二氧化碳的性质,属基础性知识考查题.


科目:初中化学 来源: 题型:选择题
| A. | 3Cl──3个铝原子 | B. | 2O──2个氧元素 | ||
| C. | H2──2个氢原子 | D. | 5S 2-──5个硫离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 30℃时,氯化铵和硫酸钠的溶解度相同,那么它们的饱和溶液中溶质的质量分数也相同 | |
| B. | 45℃时,要配制等质量的氯化铵和硫酸钠的饱和溶液所需水的质量:氯化铵>硫酸钠 | |
| C. | 将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出 | |
| D. | 将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 常温下,H2O2分解生成O2的速率较为缓慢.研究性学习小组选择“H2O2 分解生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
常温下,H2O2分解生成O2的速率较为缓慢.研究性学习小组选择“H2O2 分解生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:| 实验编号 | ① | ② |
| 反应物 | 5%H2O2 100mL | 5%H2O2 100mL |
| 加入固体 | 氯化钠固体 | 0.5g二氧化锰 |
| 收集气体所需时间 | 165s | 46s |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KNO3(NaCl):蒸发结晶 | |
| B. | CO(CO2):点燃 | |
| C. | FeSO4溶液(CuSO4溶液):过量的铁,过滤 | |
| D. | CaCO3(CaCl2):溶解,过滤,蒸发结晶 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
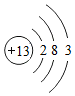 (1)用正确的化学用语填空:
(1)用正确的化学用语填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com