
【题目】某工厂欲从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
回答下列问题:
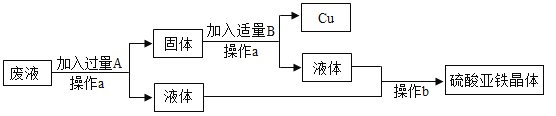
(1)操作a和操作b共同用到一种玻璃仪器是____,它在操作b中的作用____
(2)A、B物质的名称:A为_____,B为____
(3)A与废液主要成分反应的化学方程式为_____
(4)金属回收的意义____
【答案】玻璃棒 搅拌,防止局部温度过高,造成液体飞溅 铁粉 稀硫酸 Fe+CuSO4═FeSO4+Cu 节约金属资源等
【解析】
(1)操作a和操作b分别是过滤、蒸发操作,共同用到一种玻璃仪器是玻璃棒,它在操作b中的作用搅拌,防止局部温度过高,造成液体飞溅。
(2)从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,则A为铁粉,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜;得到的固体B中含有铜和过量的铁,铁能与适量的稀硫酸反应生成硫酸亚铁溶液和氢气,则B为稀硫酸。
(3)A与废液主要成分反应,即铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu。
(4)回收废旧金属,可以节约金属资源和冶炼金属消耗的能源。
故答案为:
(1)玻璃棒,搅拌,防止局部温度过高,造成液体飞溅;
(2)铁粉;稀硫酸;
(3)Fe+CuSO4═FeSO4+Cu;
(4)节约金属资源等。


 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:
【题目】氨气是重要的化工原料。
资料1:氨气是一种有刺激性气味,密度小于空气,极易溶于水的气体。
资料2:氨气能使湿润的红色石蕊试纸变蓝色。
资料3:实验室制备氨气的方法:①浓氨水滴入生石灰中;
②熟石灰和氯化铵固体混合加热。
探究一 气体制备
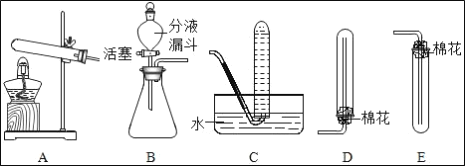
(1)若采用资料3中方法①制取氨气,发生装置可选用图1中_____装置(填序号),收集氨气选用_____装置(填序号),检验试管中已集满氨气的方法是_____。
(2)若采用资料3中方法②来制取氨气,其发生装置若用来制取氧气,写出制取氧气反应的化学方程式_____。
探究二 氨气测定
(3)实验室常用稀硫酸来吸收氨气(NH3),生成硫酸铵[(NH4)2SO4],写出该反应的化学方程式:_____。
(4)用上述原理和图2实验装置测定某公厕中氨气含量平均值。
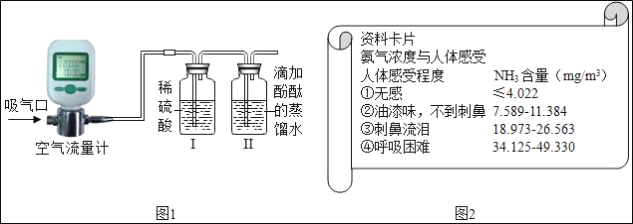
经过较长时间不间断的测定共吸取2m3的空气,最后称得Ⅰ装置增重了40mg。该公厕空气属于人体感受_____(填序号) 程度。某同学认为测得结果与自身感受不相符,请你分析产生这一误差的可能原因:_____。
探究三 氨气用途
研究人员发现氨气还可用来制作新型燃料电池,其制作工艺流程如图3。
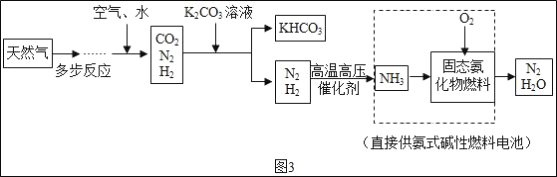
(5)该流程中可重复利用的物质是_____(写一种)。
(6)步骤①加入K2CO3溶液的作用是除去CO2,写出该反应的化学方程式_____。
(7)从环保角度看,直接供氨式碱性燃料电池的优点有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
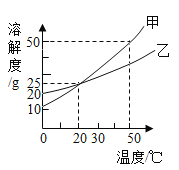
A.20℃时,100g甲溶液中含甲物质的质量小于25g
B.20℃时,等质量甲、乙饱和溶液中含溶质的质量相等
C.30℃时,甲物质的溶解度大于乙物质的溶解度
D.50℃时,将甲、乙两种物质的饱和溶液分别降温至20℃,析出晶体的质量甲大于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】资源利用与社会可持续发展密切相关。
(1)水是一种生活中不可缺少的物质。
①下列能溶于水形成溶液的是_______(填字母序号,下同),所得溶液pH>7的是______;
a 纯碱 b 蔗糖 c 面粉 d 食用油
②生活中可以采用____________方法降低水的硬度;
(2)煤的气化和液化是实现能源清洁化的重要途径。水煤气中H2和CO在加热、加压和催化剂条件下可以合成液体燃料甲醇(CH3OH),该反应中H2和CO的质量比为___________。水煤气(H2和CO)在不同催化剂的作用下,还可以合成其他物质。仅以其为原料不可能化合得到的物质是__________ (填字母序号);
a 草酸(H2C2O4) b 乙酸(C2H4O2) c 尿素[CO(NH2)2]
(3)金属钯是稀有的贵重金属之一。现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动性。
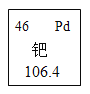
①在元素周期表中,钯元素的信息如图所示,对图中信息解释不正确的是__________;
a 原子序数为46 b 质子数为46 c 相对原子质量为46
②把钯戒指放入稀硫酸中,戒指完好无损,可推测钯在金属活动性顺序表中位于铁之________(填“前”或“后”);
③如图所示,将银、铂戒指分别放入甲、乙两试管溶液中,一段时间后取出,发现只有银戒指表面有明显变化。通过该实验判断,银、铂、钯的金属活动性由强到弱顺序为______________(用元素符号表示);

④将钯粉置于盐酸中,边通入氧气边搅拌,钯粉溶解得到二氯化钯(PdCl2)溶液,该反应的化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示某个化学反应,据图分析判断,下列说法正确的是
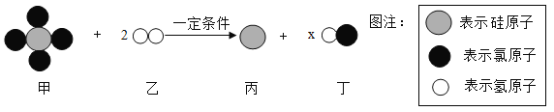
A.该图示不符合质量守恒定律B.反应前后氢元素的化合价没有发生改变
C.图示中x的数值为2D.该反应中,没有发生变化的微粒是Si、Cl、H
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图:
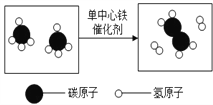
有关转化的说法正确的是( )
A. 催化剂反应前后质量不变,作用只能是加快反应
B. 该反应的化学方程式是:2CH4 = C2H4 + 2H2
C. 反应前后分子的种类发生了改变,是分解反应
D. 保持氢气化学性质的最小粒子是H
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】菱铁矿的主要成分是FeCO3.下列有关说法正确的是( )
A. 菱铁矿是铁的合金
B. 菱铁矿中铁元素的质量分数为48.3%
C. FeCO3中铁的化合价为+3
D. FeCO3是含有氧元素的化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:请你仔细分析此关系图,并进行计算。
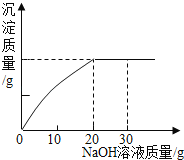
(1)当滴入氢氧化钠溶液_____g时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液的溶质的质量分数(写出计算过程)。__________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定温度下,向20g Na2CO3和NaCl的固体混合物中加入101g水,溶解后,再向其中加入100g CaCl2溶液恰好完全反应,过滤,所得滤液的质量为211g,将滤渣洗涤、干燥,称其质量为m,试计算:

(1)m=______g。
(2)求加入的CaCl2溶液中溶质的质量分数为____________?
(3)当恰好完全反应时,所得溶液中溶质的质量分数为____________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com