
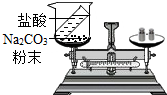
 质量守恒定律的定量研究对化学科学发展具有重大作用.
质量守恒定律的定量研究对化学科学发展具有重大作用.分析 (1)根据质量守恒定律进行分析判断.
(2)反应中没有气体参加,所以放在敞口的烧杯中进行实验,反应前后烧杯内物质质量也不变.
(3)根据用实验来验证质量守恒定律,那么结果不外乎两个:相等(当没有气体参加或不生成气体时)、不相等 (当有气体参加或生成气体时)解答.
解答 解:(1)依据化学反应前后原子的种类、数目不发生改变:N原子前后均为4,故R中无N原子;反应前有12个H原子,而NO中无H原子,故“6R”中有12个H原子,每个R中有2个H原子;同理可得每个R中含1个O原子,即化学式为:H2O
(2)因为反应过程中没有气体放出,所以反应前后烧杯中物质质量相等.
(3)造成天平的指针向右偏转的原因是:盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小;要验证质量守恒定律,有气体生成时,实验环境应在密闭体系中进行.
故答案为:(1)H2O;(2)=;(3)盐酸与碳酸钠粉末反应的装置不密闭,生成二氧化碳气体逸出,使左盘内质量减小;密闭.
点评 在任何与周围隔绝的体系中,不论发生何种变化或过程,其总质量始终保持不变.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:实验探究题
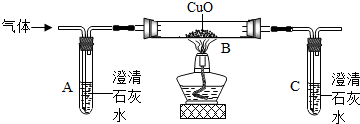 不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对其进行探究.
不少同学都被蚊虫叮咬过,感觉又痛又痒.同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤.课外兴趣小组同学决定对其进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钠原子和钠离子具有相同的质子数 | |
| B. | 洗洁精能洗去油污是因为它能溶解油污 | |
| C. | 酸碱中和后溶液不一定呈中性 | |
| D. | 有发热、发光现象的不一定是燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
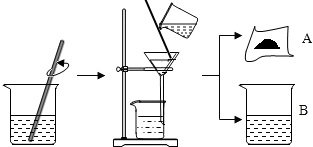 据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 自己的猜想正确 |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加(1)酚酞试液 | 溶液由无色变为红色 | 自己的猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 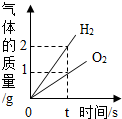 水的电解 | B. | 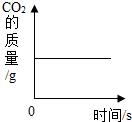 木炭在密闭容器中燃烧 | ||
| C. | 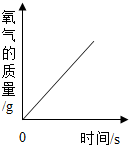 加热一定量的高锰酸钾制氧气 | D. | 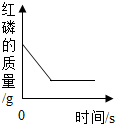 过量红磷测定空气中氧气含量 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.
碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH, 而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入氯化钙溶液 | 产生白色沉淀 | 固体产物是Na2CO3, 而不是NaOH |
| 实验三:取少量反应后的固体产物,加入过量稀盐酸(或稀硫酸、稀硝酸、醋酸) | 产生大量气泡 | 固体产物是Na2CO3, 而不是NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 1 | 20 | 15 | 8 |
| 反应后质量/g | m | 11 | 30 | 2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com