
【题目】对下列化学用语中数字“2”含义的说法正确的是( )
①2H ②2NH3 ③SO2 ④![]() ⑤Mg2+ ⑥2OH- ⑦H2O
⑤Mg2+ ⑥2OH- ⑦H2O
A. 表示离子个数的是⑤⑥B. 表示分子中原子个数的是③⑦
C. 表示离子所带电荷数的是④⑤D. 表示分子个数的是①②
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:
【题目】1.6g某物质在空气中完全燃烧生成4.4g二氧化碳和3.6g水,则关于这种物质的组成描述不正确( )
A. 该物质只含有碳元素和氢元素
B. 该物质中碳元素与氢元素的质量比为3:1
C. 该物质一定含有碳元素和氢元素,可能含有氧元素
D. 该物质的分子中碳原子与氢原子的个数比为1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图:

【甲组】氢氧化钠与硫酸铜反应的化学方程式为 ,加热后产生黑色的氧化铜。
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:
6NaOH+4CuSO4 3Na2SO4+Cu4(OH)6SO4 ↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因作出以下猜想:
猜想Ⅰ:硫酸铜溶液呈酸性; 猜想Ⅱ:生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH (填“﹥”、“﹤”或“﹦”),硫酸铜溶液呈酸性,猜想Ⅰ成立。
实验②:向盛有硫酸钠溶液的试管中逐滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈 (填“酸”、“中”或“碱”)性,猜想Ⅱ不成立。
【交流和反思】
(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是 ;
(2)在化学反应中,相同的反应物因质量比不同可能会导致生成物不同,请另举一列 (写出反应物即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用下列如图所示的装置制取气体,请你根据所学知识回答下列问题。
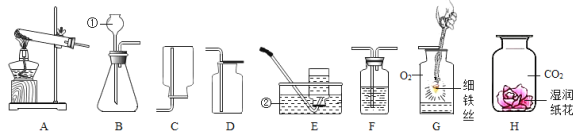
(1)指出标号仪器的名称:① ,② 。
(2)用高锰酸钾制取氧气的化学方程式为 ,应选择的发生装置是 ,可以用E装置收集氧气的原因是 ,当观察到 的现象时,说明氧气已收集满,集满氧气的集气瓶应 (填“正”或“倒”)放在桌面上.
(3)制取并收集一定量的二氧化碳,就选择的装置是 ;欲制得干燥的二氧化碳,还需将气体通过盛有 (填药品名称)的洗气瓶F.
(4)用收集到的氧气与二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛少量水的原因是 ,H中喷有紫色石蕊溶液的纸花显 色.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是a、b、c三种物质(均不含结晶水)的溶解度曲线。

①t1℃时物质的溶解度a b(填“>”或“<”或“=”);
②t2℃时将28g a物质加入到50g水中充分溶解,所得溶液的质量为 g,其中溶质与溶剂的质量比为 ;
③t1℃时,欲将c物质在m点对应的溶液变为p点的溶液,可采用的方法是 (写一种即可);
④t2℃时,将等质量的a、b、c三种物质的饱和溶液分别降温到t1℃时,所得溶液中的各项关系符合b>a>c的是 (填序号)。
Ⅰ.溶质质量 Ⅱ.溶剂质量 Ⅲ.溶液质量 Ⅳ.溶质的质量分数
⑤欲配置100g质量分数为15%的a物质的溶液,所需a物质 g,所需蒸馏水的体积为 mL,可选择的量筒规格为 mL(填50或100),溶解时玻璃棒的作用是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】《2015年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。下列是我国能源结构变化的调整图,请回答相关问题:

(1)化石燃料是目前应用最广泛的能源,但不可再生且燃烧会对环境造成污染。化石燃料包括煤、石油和_____;
(2)从2015、2030、2050年能源结构变化看,所占比例增加最多的是_____;
(3)在新能源开发中,化学发挥着不可替代的作用。近年,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过下图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中c、d是最终制得的汽油中所含物质的分子结构模型)。
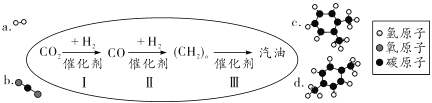
①在一定温度、一定压强和催化剂存在的条件下,环节I除生成CO外,还生成了一种化合物,则反应的化学方程式为_____;
②观察图中c和d两种物质的分子结构模型,发现c和d的分子组成完全相同,但其分子结构不同,化学上将其称为同分异构体。你认为c和d的化学性质_____(填“是”或“否”)完全相同。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定金属镁样品中镁的质量分数(杂质不含镁元素,不溶于水,也不与其它物质发生反应),进行了如下实验:请回答下列问题:
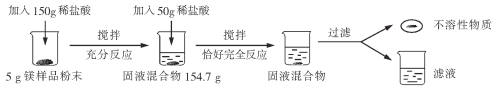
(1)上述实验过程中发生反应的化学方程式为________________________________。
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质质量(x)的比例式________________。
(3)此镁样品中镁的质量分数为________________。
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需浓盐酸的质量为________________。
(5)若将反应后的滤液蒸发104.4g水,无晶体析出,所得溶液中溶质的质量分数为__________。
(6)若要生产含镁4.5%的铝合金960t,需要上述金属镁样品的质量为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com