
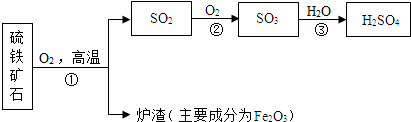
分析 二氧化硫和三氧化硫都属于氧化物;
二硫化亚铁和氧气在高温条件下反应生成氧化铁和二氧化硫;
根据提供的数据可以进行相关方面的计算;
氢氧化钠能和二氧化硫反应生成亚硫酸钠和水.
解答 解:(1)流程图所涉及的含硫物质中硫元素的最低价是二硫化亚铁中硫元素的化合价,是-1价,属于氧化物的是SO2,SO3.
故填:-1;SO2,SO3.
(2)反应①的化学方程式为:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2.
故填:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2.
(3)设至少需要含杂质30%的矿渣的质量为x,
根据题意有:x×(1-30%)×$\frac{112}{160}$×100%=100t×98%,
x=200t,
故填:200.
(4)生产产生的尾气中,可能存在的大气污染物是SO2;
下列物质能用于吸收该污染物的是氢氧化钠溶液.
故填:SO2;②.
点评 虽然澄清石灰水也能够吸收二氧化硫,但是由于氢氧化钙的溶解度很小,因此不能用于吸收二氧化硫.


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
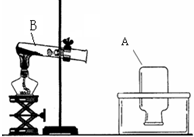 绘制实验装置图是我们初中生应该掌握的一项技能.图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请按要求回答下列问题.
绘制实验装置图是我们初中生应该掌握的一项技能.图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请按要求回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
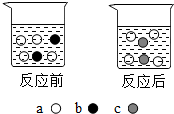 含有相同离子的盐也具有相似的化学性质
含有相同离子的盐也具有相似的化学性质查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气占空气质量的21% | |
| B. | 好酒不怕巷子深,是由于分子的不断运动 | |
| C. | 催化剂在化学变化前后质量和性质保持不变 | |
| D. | 氧气可用于食品保鲜 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
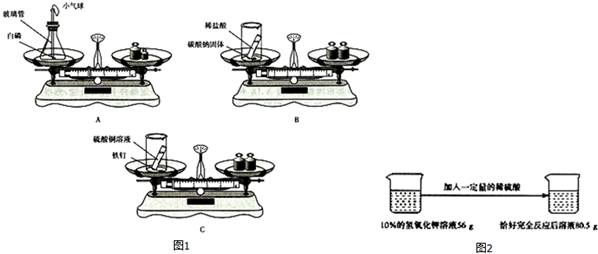
| 物质 | A | B | C | D |  氮原子 氮原子 氧原子 氧原子 氢原子 氢原子 |
| 微观示意图 |  |  |  |  | |
| 反应前质量/g | 100 | 20 | X | y | |
| 反应后质量/g | 32 | 140 | 126 | 46 |
| 温度(℃) | 25 | 350 | 400 | 500 | 600 | 900 |
| 固体质量(g) | 0.80 | 0.80 | 0.40 | 0.44 | 0.44 | 0.43 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com