
分析 根据质量守恒定律,化学反应前后物质的总质量不变,向碳酸钠和氯化钠的固体混合物中加入稀盐酸,只是碳酸钠与盐酸反应,反应后生成了二氧化碳气体不存在于溶液中,可以求得二氧化碳的质量;依据二氧化碳的质量利用方程式可以求出碳酸钠的质量,进而可求碳酸钠的质量分数.
解答 解:(1)由质量守恒定律可知,生成的二氧化碳的质量=10g+92.2g-100g=2.2g;
(2)设原固体混合物中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{44}=\frac{x}{2.2g}$ 解得:x=5.3g
样品中纯碱的质量分数:$\frac{5.3g}{10g}×$100%=53%
故答为:(1)2.2;(2)计算样品中纯碱的质量分数是53%.
点评 本题通过计算的形式考查了碳酸盐与酸的反应,解答本题的关键是根据质量守恒定律来进行计算是要计算生成的二氧化碳的质量.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | D. | Fe+CuSO4═FeSO4+Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
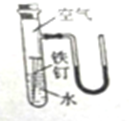 如图是某研究的实验装置,几天以后:
如图是某研究的实验装置,几天以后:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
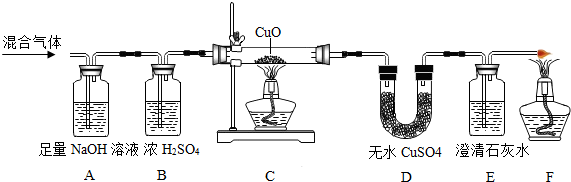
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com