

分析 (1)根据铁生锈的条件解答;
(2)控制变量设计实验;
(3)根据所给资料二分析解释;
(4)根据防锈原理解答;
(5)根据铝的自我保护分析.
(6)根据防锈方法解答.
(7)根据质量守恒定律,溶液减少的质量为氢气的质量,结合化学方程式计算参加反应的铁的质量,进一步计算已生锈的铁的质量及质量分数.
解答 解:(1)铁生锈的条件是铁与空气中的水分和氧气共同作用的结果,A中铁钉满足铁生锈的条件,一段时间后会出现明显的锈迹.
(2)将A装置中的氧气换做氮气或二氧化碳就可验证空气中氮气或二氧化碳有没有参加铁生锈的反应.
(3)因为导电的溶液可加速铁的生锈,硫酸钠溶液中含有钠离子和硫酸根离子,如果把蒸馏水换为硫酸钠溶液可使铁生锈速率加快.
(4)铁比锡活泼,锡层破坏后,铁锈蚀速度加快.
(5)大门上刷一层银白色金属,该金属可能是镁,因为镁在空气能形成一层致密坚固的氧化镁薄膜,隔绝水分和氧气,起到防锈作用.
(6)铁制品防锈的方法有涂保护层,刷油漆等.
(7)解:生成氢气的质量为10g+100g-109.9 g=0.1 g
设还没有生锈的铁的质量为x.
Fe+H2SO4=FeSO4+H2↑
56 2
X 0.1 g
$\frac{56}{X}=\frac{2}{0.1g}$
X=2.8 g
则已生锈的铁的质量为(10g-2.8 g)×70%=5.04 g
原铁块中已经生锈的铁的质量分数为:$\frac{5.04g}{2.8g+5.04g}×100%$=64.3%.
故答案为:
(1)A;氧气和水蒸气;
(2)将A装置中的氧气换作氮气或二氧化碳;
(3)a;(4)b;(5)c;(6)刷油漆.(其他合理答案均可)
(7)64.3%.
点评 该题的难点是根据所给的资料信息提炼出有用的信息并运用到题目中解题.如资料一:导电的溶液可加速铁生锈,这里就要知道什么样的溶液易导电,一般是溶液电离出阴阳离子的溶液,如氯化钠溶液、硫酸钠溶液等;资料二:轮船上镶嵌锌块,防止钢的腐蚀,说明活泼的金属更易腐蚀.提炼出这些信息,解题就不难了


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 操作 | 装置 | 现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上. | 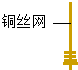 | / |
| 2、分别向①和②中注入15mL30%的过氧化氢溶液,并放入盛有热水的③中. | 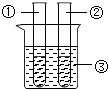 | 约1分钟后可观察到①和②中都有少量气泡产生 |
| 3、把铜丝插入①中. | 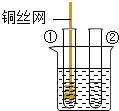 | ①中有大量气泡产生,约分钟后不再有气泡产生;此时②中 仍然有少量气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示的是A、B、C三种固体物质的溶解度曲线.
如图所示的是A、B、C三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 组别编号 | 样品质量(g) | 加入稀硫酸质量(g) | 剩余固体质量(g) |
| 烧杯① | 10 | 10 | 9.2 |
| 烧杯② | 10 | 20 | 8.4 |
| 烧杯③ | 10 | 30 | 8 |
| 烧杯④ | 10 | 40 | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com